¿Qué es la enfermedad de Parkinson?
La enfermedad de Parkinson (EP) es una afección neurodegenerativa crónica y progresiva que afecta predominantemente al sistema motor. Es la segunda enfermedad neurodegenerativa más frecuente del mundo, solo por detrás de la enfermedad de Alzheimer.
La enfermedad se debe a la degeneración progresiva de las neuronas dopaminérgicas de la sustancia negra del mesencéfalo. La pérdida de estas neuronas reduce la disponibilidad de dopamina en los ganglios de la base, circuitos cerebrales esenciales para el control fino del movimiento voluntario.
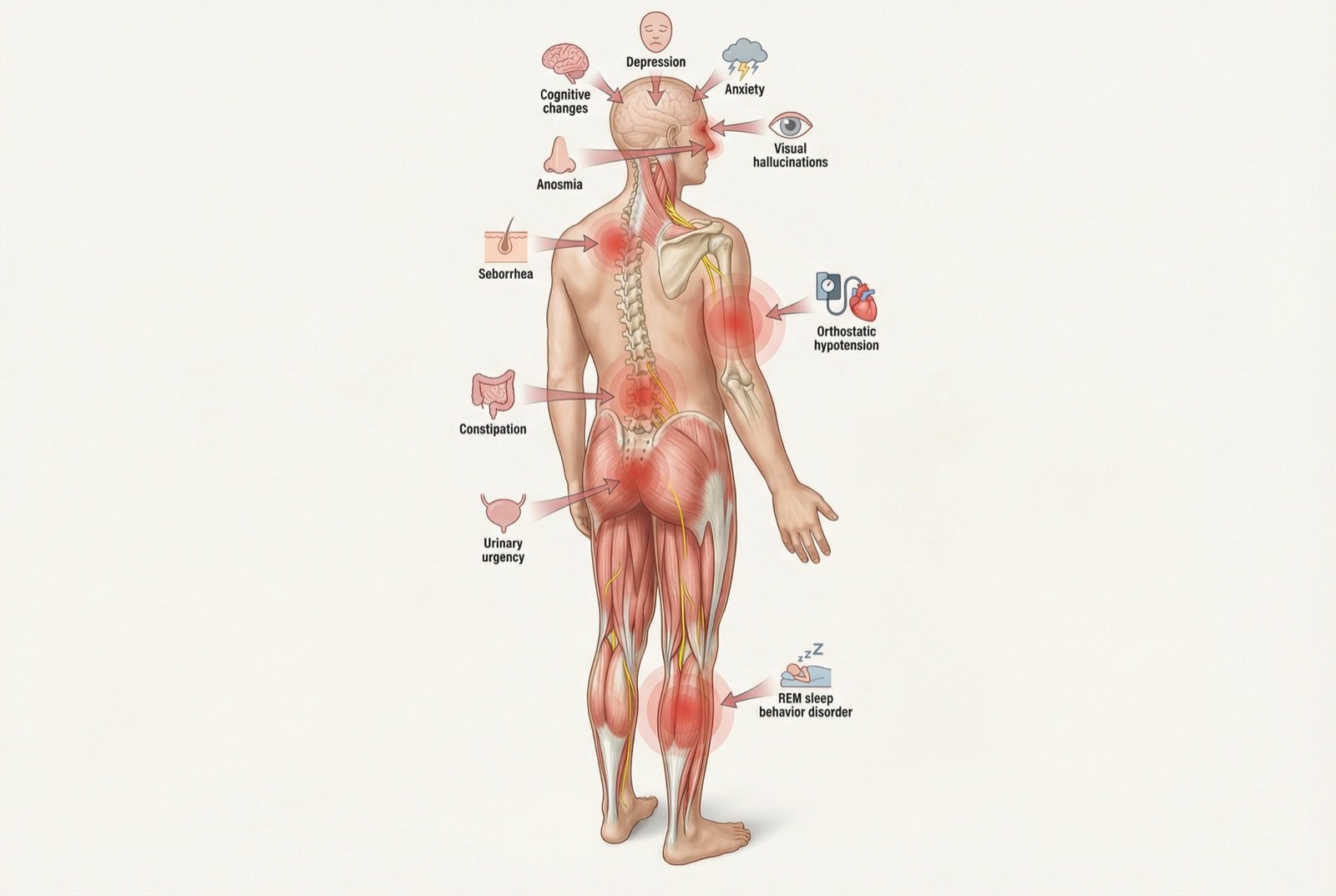
Aunque clásicamente se ha descrito como un trastorno motor, hoy la EP se reconoce como una enfermedad multisistémica. Los síntomas no motores — como trastornos del sueño, depresión, estreñimiento y pérdida del olfato — preceden con frecuencia a los síntomas motores en años o incluso décadas.
Degeneración dopaminérgica
La pérdida de las neuronas productoras de dopamina en la sustancia negra es el mecanismo central de la enfermedad.
Más allá del movimiento
Los síntomas no motores como depresión, estreñimiento y trastornos del sueño forman parte integral de la enfermedad.
Progresión gradual
La enfermedad evoluciona lentamente a lo largo de los años. Los síntomas motores aparecen cuando ya se ha perdido el 60-80 % de las neuronas dopaminérgicas.
Epidemiología
La enfermedad de Parkinson afecta aproximadamente al 1-2 % de la población mayor de 60 años, con incidencia creciente con la edad. Es algo más prevalente en hombres que en mujeres, con una proporción aproximada de 1,5:1. La edad media de inicio se sitúa entre los 55 y los 65 años, aunque las formas de inicio precoz (antes de los 40 años) suponen el 5-10 % de los casos.
Los factores de riesgo establecidos incluyen edad avanzada, sexo masculino, antecedentes familiares y exposición a plaguicidas o herbicidas. Curiosamente, el consumo de cafeína y el tabaquismo se asocian a un menor riesgo — aunque el tabaquismo no se recomienda por sus otros riesgos para la salud.
Fisiopatología
El mecanismo central de la EP es la degeneración de las neuronas dopaminérgicas de la pars compacta de la sustancia negra. Estas neuronas se proyectan al estriado (caudado y putamen) y forman la vía nigroestriatal, esencial para la modulación del movimiento voluntario.
La marca histopatológica de la enfermedad son los cuerpos de Lewy — inclusiones citoplasmáticas compuestas predominantemente por alfa-sinucleína agregada. La hipótesis de Braak propone que la patología por alfa-sinucleína se disemina de forma ascendente, comenzando en el bulbo olfatorio y el sistema nervioso entérico, progresando al tronco encefálico y, por último, alcanzando la corteza cerebral.

La dopamina equilibra normalmente la actividad de dos vías de los ganglios de la base: la vía directa (que facilita el movimiento) y la vía indirecta (que inhibe los movimientos innecesarios). La depleción dopaminérgica produce hipoactividad de la vía directa e hiperactividad de la vía indirecta, lo que ocasiona bradicinesia y rigidez.
Los mecanismos celulares implicados en la neurodegeneración incluyen disfunción mitocondrial, estrés oxidativo, neuroinflamación mediada por la microglía, disfunción del sistema ubiquitina-proteasoma y agregación patológica de alfa-sinucleína. Los factores genéticos (mutaciones en SNCA, LRRK2, Parkin, PINK1) y ambientales interactúan para determinar el riesgo individual.
Síntomas
Los síntomas motores clásicos de la EP suelen resumirse con el acrónimo TRAP: temblor de reposo, rigidez, acinesia/bradicinesia e inestabilidad postural. El inicio es típicamente asimétrico y afecta a un lado del cuerpo antes que al otro.
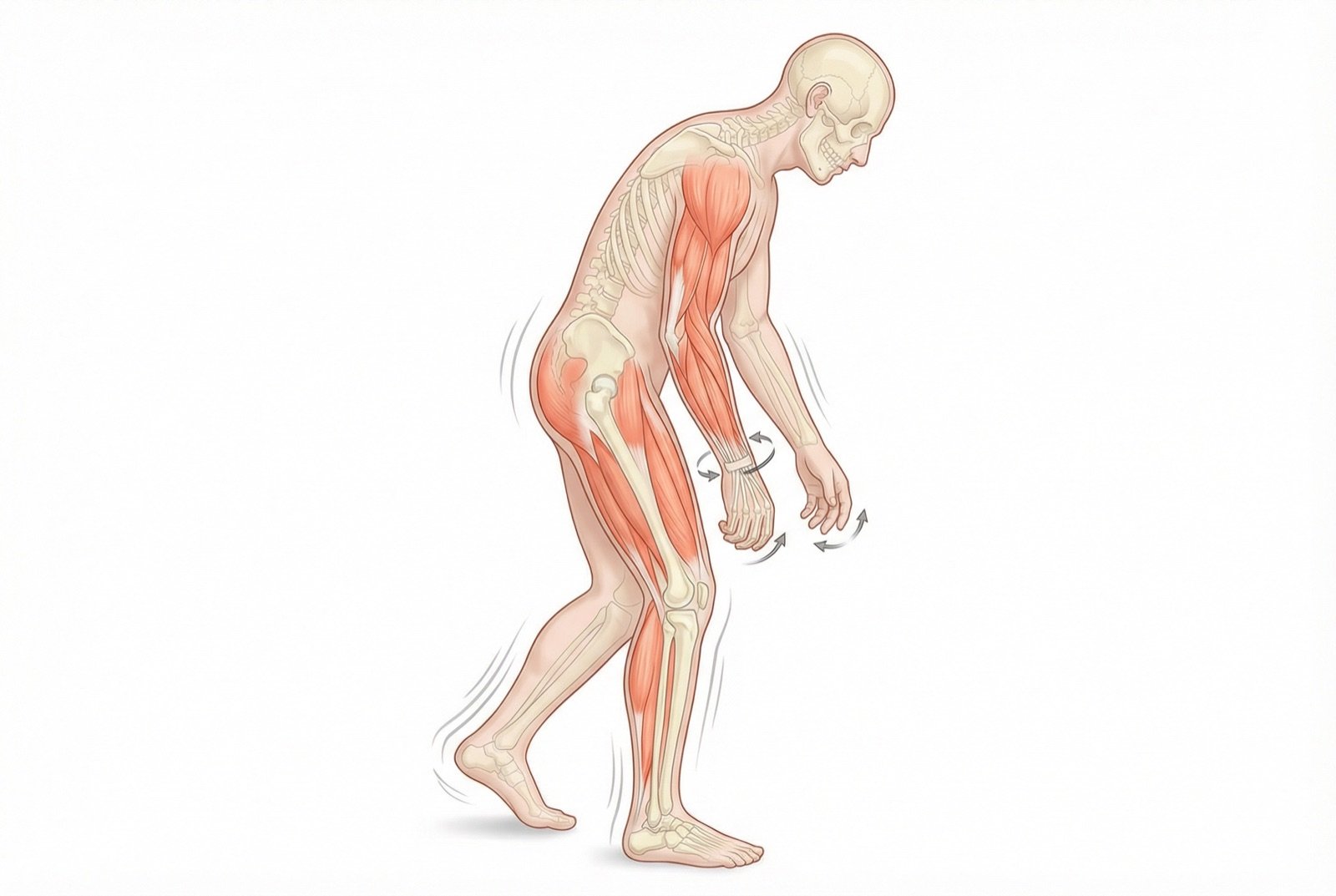
Síntomas motores cardinales
- 01
Temblor de reposo
Temblor rítmico de 4-6 Hz, típicamente en «contar billetes» o «hacer rodar una píldora». Comienza en una mano y es más evidente en reposo, y disminuye con el movimiento voluntario.
- 02
Bradicinesia
Lentitud progresiva de los movimientos. Micrografía (letra cada vez más pequeña), hipomimia (reducción de la expresión facial) y disminución del balanceo de los brazos al caminar.
- 03
Rigidez
Aumento del tono muscular en «rueda dentada» — resistencia entrecortada al movimiento pasivo. Está presente en miembros, tronco y cuello.
- 04
Inestabilidad postural
Pérdida de los reflejos posturales, tendencia a las caídas. Suele aparecer en estadios más avanzados de la enfermedad.
- 05
Marcha festinante
Pasos cortos y arrastrados con aceleración involuntaria. Dificultad para iniciar la marcha (freezing) y para girar.
- 06
Hipofonía
Reducción del volumen y monotonía de la voz, lo que dificulta la comunicación.
Síntomas no motores
- 01
Hiposmia/anosmia
Pérdida parcial o total del olfato — puede preceder a los síntomas motores en años.
- 02
Trastorno conductual del sueño REM
El paciente «representa» los sueños durante el sueño REM y puede dar patadas, golpes o gritar. Predictor potente de futura EP.
- 03
Estreñimiento
Disminución de la motilidad intestinal, frecuentemente presente años antes del diagnóstico motor.
- 04
Depresión y ansiedad
Afectan al 40-50 % de los pacientes. Se relacionan tanto con la neuroquímica de la enfermedad como con el impacto funcional.
- 05
Disfunción cognitiva
Lentitud del procesamiento, dificultad ejecutiva. La demencia puede aparecer en estadios avanzados.
- 06
Hipotensión ortostática
Caída de la presión arterial al levantarse, que provoca mareo o desmayo. Refleja disfunción autonómica.
Diagnóstico
El diagnóstico de la enfermedad de Parkinson es esencialmente clínico, basado en la historia y la exploración neurológica. No existe una prueba de laboratorio o de imagen que confirme definitivamente la enfermedad en vida. El criterio diagnóstico central es la presencia de bradicinesia asociada a temblor de reposo o rigidez.
Las pruebas de imagen como la resonancia magnética cerebral son normales en la EP, pero resultan útiles para descartar otras causas. El DaTSCAN (gammagrafía del transportador de dopamina) puede mostrar una reducción de la captación dopaminérgica en el estriado y ayudar al diagnóstico diferencial con el temblor esencial.
🏥Criterios diagnósticos MDS (Movement Disorder Society)
Fonte: Postuma et al., 2015 — MDS Clinical Diagnostic Criteria
Criterio esencial
Obligatorio para el diagnóstico.- 1.Parkinsonismo: bradicinesia + temblor de reposo y/o rigidez.
Criterios de apoyo
- 1.Respuesta clara y dramática a la terapia dopaminérgica.
- 2.Presencia de discinesias inducidas por levodopa.
- 3.Temblor de reposo documentado en un miembro.
- 4.Pérdida olfatoria o denervación cardíaca en la gammagrafía MIBG.
Criterios de exclusión absoluta
- 1.Signos cerebelosos inequívocos.
- 2.Parálisis supranuclear de la mirada vertical.
- 3.Diagnóstico de demencia frontotemporal o afasia progresiva primaria.
- 4.Parkinsonismo restringido a los miembros inferiores durante más de 3 años.
- 5.Uso de bloqueantes dopaminérgicos (parkinsonismo medicamentoso).
DIAGNÓSTICO DIFERENCIAL DEL PARKINSONISMO
| AFECCIÓN | CARACTERÍSTICAS DISTINTIVAS | RESPUESTA A LA LEVODOPA |
|---|---|---|
| Enfermedad de Parkinson | Asimétrica, temblor de reposo, progresión lenta. | Excelente |
| Temblor esencial | Temblor de acción/postural, bilateral, antecedentes familiares. | Ninguna |
| Parálisis supranuclear progresiva | Parálisis de la mirada vertical, caídas precoces, rigidez axial. | Pobre |
| Atrofia multisistémica | Disautonomía grave, signos cerebelosos. | Pobre a moderada |
| Parkinsonismo vascular | Marcha predominante, sin temblor, factores de riesgo vascular. | Pobre |
| Parkinsonismo medicamentoso | Simétrico, uso de antipsicóticos/metoclopramida. | Variable (se resuelve al suspenderlo). |
Diagnóstico diferencial
El parkinsonismo — síndrome de bradicinesia, rigidez y temblor — puede tener diversas causas además de la enfermedad de Parkinson idiopática. El diagnóstico correcto es esencial, pues el tratamiento y el pronóstico difieren significativamente.
DIAGNÓSTICO DIFERENCIAL
Diagnóstico diferencial
Temblor esencial
- Temblor de acción (no de reposo)
- Bilateral, simétrico
- Sin rigidez ni bradicinesia
- Antecedentes familiares
Pruebas diagnósticas
- Exploración neurológica
- DaTscan si es necesario
Parkinsonismo secundario a fármacos
- Uso de bloqueantes dopaminérgicos
- Metoclopramida, haloperidol
- Bilateral y simétrico
Pruebas diagnósticas
- Anamnesis farmacológica
- Mejoría tras la suspensión
Atrofia multisistémica
- Disfunción autonómica precoz
- Caídas frecuentes
- Respuesta pobre a la levodopa
Pruebas diagnósticas
- RM (atrofia putaminal)
- Pruebas autonómicas
Parálisis supranuclear progresiva
- Caídas precoces hacia atrás
- Mirada vertical alterada
- Postura erguida (no encorvada)
Pruebas diagnósticas
- RM (signo del pingüino)
- Exploración de la mirada vertical
Parkinsonismo vascular
- Marcha festinante más que temblor
- Lesiones isquémicas en la sustancia blanca
- Respuesta pobre a la levodopa
Pruebas diagnósticas
- RM con lesiones lacunares
Enfermedad de Parkinson vs. temblor esencial
El temblor esencial es el diagnóstico diferencial más frecuente en la práctica clínica. La distinción es fundamental porque el tratamiento es completamente distinto. Las principales diferencias: el temblor de la EP es de reposo (aparece cuando el miembro está en reposo y disminuye con el movimiento voluntario), mientras que el temblor esencial es de acción/postural (aparece al sostener una postura o durante el movimiento). La EP es unilateral o asimétrica al inicio; el temblor esencial es bilateral y simétrico. La EP cursa con bradicinesia y rigidez obligatorias; el temblor esencial no. Los antecedentes familiares son más frecuentes en el temblor esencial. El DaTscan muestra captación dopaminérgica reducida en la EP y normal en el temblor esencial, lo que puede resolver casos dudosos.
El parkinsonismo inducido por fármacos a menudo está infradiagnosticado. La metoclopramida (utilizada para las náuseas y la gastroparesia), el haloperidol, la risperidona, la quetiapina y otros antipsicóticos bloquean los receptores dopaminérgicos y pueden causar un parkinsonismo clínicamente idéntico a la EP idiopática. La característica distintiva es que el parkinsonismo medicamentoso es típicamente bilateral y simétrico (a diferencia de la EP, que es asimétrica). La revisión cuidadosa de los medicamentos en uso y la mejoría tras la suspensión confirman el diagnóstico. El DaTscan es normal en el parkinsonismo medicamentoso.
Atrofia multisistémica y PSP: parkinsonismos atípicos
La atrofia multisistémica (AMS) y la parálisis supranuclear progresiva (PSP) reciben el nombre de «parkinsonismos atípicos» o «síndromes Parkinson-plus». Tienen peor pronóstico que la EP y responden poco a la levodopa — un elemento clínico importante. La AMS se caracteriza por disfunción autonómica precoz y prominente (hipotensión ortostática grave, disfunción sexual, incontinencia urinaria) y, con frecuencia, signos cerebelosos. La PSP tiene como rasgos distintivos: caídas hacia atrás precoces (ya en el primer año), parálisis de la mirada vertical (incapacidad para mover los ojos hacia arriba y abajo), postura axial erguida (el paciente con EP tiende a encorvarse, el de PSP permanece erguido) y ausencia de temblor.
El parkinsonismo vascular afecta de manera prominente la marcha (marcha de base ancha, pasos cortos, «marcha magnética») con menos temblor de reposo que la EP idiopática. Aparece en pacientes con múltiples factores de riesgo vascular y lesiones isquémicas extensas en la sustancia blanca en la RM. La respuesta a la levodopa es pobre. Reconocer estos parkinsonismos atípicos es importante para el asesoramiento pronóstico correcto al paciente y a la familia.
La respuesta a la levodopa como herramienta diagnóstica
La respuesta clara y sostenida a la levodopa (mejoría de al menos un 30 % en los síntomas motores) es un criterio de apoyo diagnóstico para la EP idiopática en los criterios MDS. En la práctica, el ensayo terapéutico con levodopa en dosis adecuada (escalonada según tolerancia, por lo general hasta 600-1000 mg/día en 3-4 semanas, bajo supervisión del neurólogo — las dosis iniciales más altas pueden producir hipotensión ortostática, náuseas y confusión en personas mayores) puede ayudar a distinguir la EP idiopática de los parkinsonismos atípicos. Una respuesta dramática y sostenida apoya la EP; una respuesta pobre o ausente debe aumentar la sospecha de AMS, PSP o parkinsonismo vascular.
En casos dudosos, especialmente en la distinción entre EP y temblor esencial, el DaTscan (gammagrafía del transportador de dopamina) muestra reducción de la captación en el estriado en la EP y es normal en el temblor esencial y en el parkinsonismo medicamentoso. Es una prueba de coste elevado, pero puede ser decisiva en casos clínicamente ambiguos.
Tratamiento
No existe un tratamiento curativo para la enfermedad de Parkinson. El objetivo terapéutico es controlar los síntomas y mantener la calidad de vida el mayor tiempo posible. El tratamiento es individualizado y considera la edad, los síntomas predominantes, el impacto funcional y las comorbilidades.
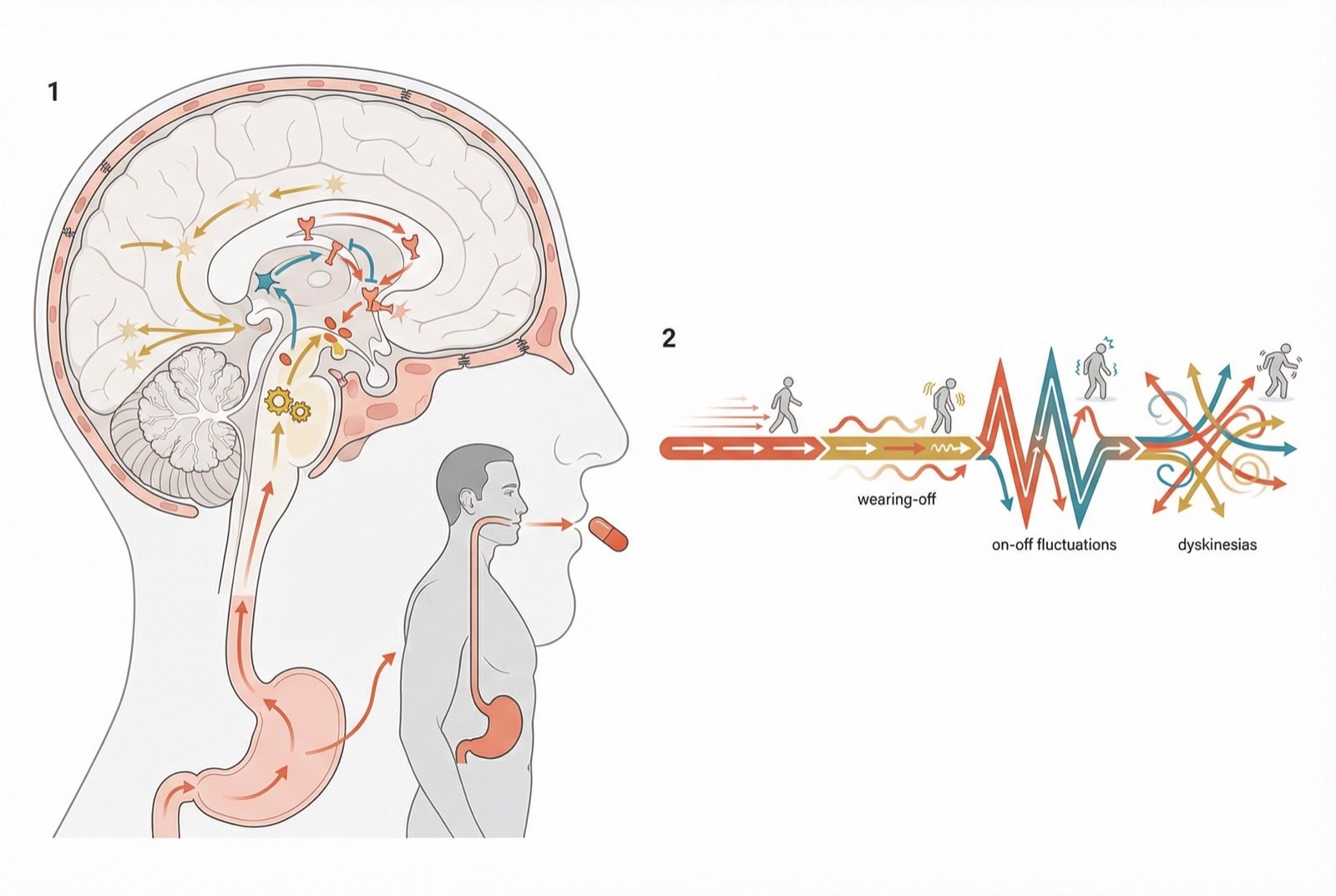
Fase inicial
Primeros 1-5 añosSíntomas leves. Puede optarse por iniciar con inhibidores de la MAO-B (rasagilina, selegilina) o agonistas dopaminérgicos en pacientes jóvenes. Levodopa en pacientes mayores o con mayor afectación funcional.
Fase de luna de miel
3-7 años de tratamientoBuena respuesta a la medicación con control estable de los síntomas. La levodopa produce una respuesta sostenida a lo largo del día.
Fase de complicaciones motoras
Tras 5-10 añosAparecen fluctuaciones motoras (wearing-off, on-off) y discinesias inducidas por levodopa. Se requieren ajustes frecuentes y terapias combinadas.
Fase avanzada
VariableSíntomas refractarios, disfagia, demencia, caídas. Considerar terapias avanzadas: estimulación cerebral profunda (DBS), infusión continua de levodopa/apomorfina.
PRINCIPALES MEDICAMENTOS PARA LA ENFERMEDAD DE PARKINSON
| CLASE | EJEMPLOS | MECANISMO | INDICACIÓN PRINCIPAL |
|---|---|---|---|
| Levodopa/carbidopa | Sinemet, Stalevo | Precursor de la dopamina + inhibidor de la descarboxilasa periférica. | Tratamiento más eficaz; patrón de referencia. |
| Agonistas dopaminérgicos | Pramipexol, rotigotina | Estimulan directamente los receptores de dopamina. | Monoterapia inicial en jóvenes; adyuvante. |
| Inhibidores de la MAO-B | Rasagilina, selegilina | Inhiben la degradación de la dopamina. | Fase inicial; adyuvante para fluctuaciones. |
| Inhibidores de la COMT | Entacapona, opicapona | Prolongan la acción de la levodopa. | Fluctuaciones motoras (wearing-off). |
| Anticolinérgicos | Biperideno, trihexifenidilo | Reducen la actividad colinérgica relativa. | Temblor predominante en jóvenes. |
| Amantadina | Amantadina | Antagonista de NMDA + aumento de dopamina. | Discinesias inducidas por levodopa. |
Acupuntura como tratamiento
La acupuntura se utiliza como terapia complementaria en la enfermedad de Parkinson, no como sustituto del tratamiento farmacológico convencional. Los estudios preclínicos y clínicos sugieren beneficios potenciales en síntomas específicos, aunque la evidencia se considera todavía moderada por la comunidad científica.
Los mecanismos hipotetizados, derivados predominantemente de modelos preclínicos, incluyen una posible modulación de la liberación de dopamina en el estriado, una posible reducción de la neuroinflamación, influencia sobre factores neurotróficos (GDNF, BDNF) y modulación del eje hipotálamo-hipófisis-suprarrenal. Los estudios en modelos animales de Parkinson sugieren que la electroacupuntura puede atenuar la pérdida de neuronas dopaminérgicas en la sustancia negra — hallazgos que aún requieren validación en humanos antes de ser extrapolados a la clínica.
En la práctica clínica, la acupuntura puede ayudar en el manejo de síntomas como dolor musculoesquelético, estreñimiento, insomnio, ansiedad y fatiga — síntomas no motores que afectan significativamente a la calidad de vida y no siempre se controlan bien con la medicación.
Pronóstico
La enfermedad de Parkinson es progresiva, pero la velocidad de progresión varía considerablemente entre los pacientes. Con el tratamiento adecuado, muchos pacientes mantienen una buena funcionalidad durante 10-20 años o más. La esperanza de vida está ligeramente reducida respecto a la población general, pero ha mejorado significativamente con las terapias actuales.
Los factores asociados a un mejor pronóstico incluyen el inicio con temblor predominante, la edad joven al diagnóstico y una buena respuesta a la levodopa. Los factores asociados a peor pronóstico incluyen inestabilidad postural precoz, disfunción cognitiva, alucinaciones y edad avanzada al diagnóstico.
Mitos y hechos
Mito frente a hecho
El Parkinson es solo temblor.
El temblor es el síntoma más visible, pero la EP incluye bradicinesia, rigidez, problemas de equilibrio y un amplio espectro de síntomas no motores como depresión, estreñimiento y trastornos del sueño.
Mito frente a hecho
La levodopa debe retrasarse lo máximo posible para «ahorrar» su efecto.
La evidencia actual no respalda esa práctica. Retrasar la levodopa no prolonga su efecto a largo plazo y puede deteriorar innecesariamente la calidad de vida. Las complicaciones motoras dependen más de la progresión de la enfermedad que del tiempo de uso del medicamento.
Mito frente a hecho
La enfermedad de Parkinson solo afecta a personas mayores.
Aunque es más frecuente después de los 60 años, el 5-10 % de los casos comienzan antes de los 40 años (Parkinson de inicio precoz). Los casos juveniles, aunque infrecuentes, pueden aparecer antes de los 20 años.
Mito frente a hecho
Nada puede hacerse para retrasar la progresión.
El ejercicio físico regular es la intervención no farmacológica con evidencia más consistente de un potencial efecto neuroprotector en la EP; se trata de una asociación observacional en estudios de cohorte, no de una prueba definitiva de modificación de la enfermedad. Los ejercicios aeróbicos y actividades como el taichí muestran beneficios en la función motora y pueden influir en la progresión.
Cuándo buscar ayuda
El diagnóstico precoz de la enfermedad de Parkinson permite el inicio oportuno del tratamiento y una mejor planificación a largo plazo. Consulte a un neurólogo si presenta los siguientes signos:
Lo ideal es la evaluación por un neurólogo especializado en trastornos del movimiento para garantizar un diagnóstico preciso y un plan terapéutico individualizado. El seguimiento multidisciplinario — incluyendo fisioterapia, logopedia, terapia ocupacional y apoyo psicológico — es fundamental para optimizar la calidad de vida a lo largo de la evolución de la enfermedad.
Preguntas frecuentes
Preguntas Frecuentes
Aún no existe un tratamiento curativo para la enfermedad de Parkinson. Los tratamientos actuales — sobre todo la levodopa — controlan los síntomas y mejoran significativamente la calidad de vida, pero no detienen la progresión de la neurodegeneración. No obstante, las investigaciones en inmunoterapias frente a la alfa-sinucleína, terapia génica y células madre ofrecen perspectivas prometedoras para el futuro. El ejercicio físico es la única intervención con evidencia de un potencial efecto neuroprotector en humanos.
La evidencia actual no avala retrasar la levodopa para «ahorrar» su efecto — esa práctica no prolonga la ventana terapéutica y deteriora innecesariamente la calidad de vida. La indicación de la levodopa se basa en el impacto funcional de los síntomas: cuando la bradicinesia, la rigidez o el temblor empiezan a interferir con el trabajo, las actividades cotidianas o la calidad de vida, es momento de comenzarla. En pacientes más jóvenes (menos de 60 años) puede iniciarse con agonistas dopaminérgicos o inhibidores de la MAO-B para retrasar las complicaciones motoras de la levodopa a largo plazo.
Las fluctuaciones motoras son variaciones de la eficacia de la medicación a lo largo del día: períodos «on» (buena respuesta) y períodos «off» (regreso de los síntomas). El wearing-off es la disminución del efecto antes de la siguiente dosis. Las discinesias son movimientos involuntarios (retorcimientos, balanceos) que aparecen generalmente en el pico de efecto de la levodopa. Surgen tras 5-10 años de tratamiento con levodopa en muchos pacientes. Las estrategias de manejo incluyen: ajuste de dosis y frecuencia de la levodopa, adición de inhibidores de la COMT, agonistas dopaminérgicos, amantadina y, en casos seleccionados, estimulación cerebral profunda.
No. La estimulación cerebral profunda (deep brain stimulation) está indicada en pacientes con EP idiopática confirmada, buena respuesta previa a la levodopa, fluctuaciones motoras o discinesias incapacitantes que no responden al ajuste farmacológico, sin demencia significativa y en buenas condiciones clínicas para la cirugía. La respuesta pobre a la levodopa, la demencia y los parkinsonismos atípicos son contraindicaciones relativas. La DBS no cura la enfermedad, pero puede mejorar drásticamente la calidad de vida en pacientes seleccionados.
Sí, es una de las intervenciones con mayor nivel de evidencia en la EP. Los ejercicios aeróbicos, el entrenamiento de fuerza, el taichí, el tango argentino y la danza muestran beneficios en el equilibrio, la marcha, la bradicinesia, la fatiga y la calidad de vida. Estudios en modelos animales y en humanos sugieren efectos neuroprotectores a través de la liberación de BDNF y otros factores neurotróficos. La recomendación es de al menos 150 minutos de ejercicio aeróbico moderado a la semana, con entrenamiento adicional de equilibrio y coordinación. Los programas supervisados por profesionales con experiencia en EP son ideales.
La acupuntura puede considerarse como opción adyuvante, entre las no farmacológicas, para los síntomas no motores de la EP que con frecuencia responden parcialmente a la levodopa: dolor musculoesquelético, estreñimiento, insomnio, ansiedad y fatiga. Los metaanálisis y revisiones sistemáticas (Lee 2008 Cochrane, actualizaciones posteriores y ensayos clínicos de grupos chinos) sugieren que la acupuntura, como adyuvante al tratamiento convencional, puede mejorar las puntuaciones motoras (UPDRS) en parte de los pacientes. La calidad metodológica es heterogénea y los estudios varían en protocolo, tamaño muestral y riesgo de sesgo — los efectos no incluyen modificación del curso natural de la enfermedad. El médico acupunturista puede integrar la acupuntura en el plan terapéutico individualizado, sin sustituir la medicación dopaminérgica ni modificar la progresión neurodegenerativa.
No — la EP se reconoce hoy como una enfermedad multisistémica. Los síntomas no motores son parte integral y, con frecuencia, los más impactantes en la calidad de vida: depresión y ansiedad (40-50 %), disfunción cognitiva (puede evolucionar a demencia en el 30-40 % de los casos), trastornos del sueño (insomnio, trastorno conductual del sueño REM), estreñimiento (presente en el 80 %), hipotensión ortostática, disfunción sexual, dolor y fatiga. Estos síntomas no motores con frecuencia preceden a los motores en años.
En la mayoría de los casos no — al menos no de inmediato. El diagnóstico precoz de EP suele permitir mantener las actividades profesionales durante varios años con el tratamiento adecuado. La decisión depende del tipo de trabajo, del grado de afectación motora y de la respuesta a la medicación. Las actividades que requieren destreza manual fina, equilibrio en situaciones de riesgo o conducir profesionalmente pueden verse afectadas más pronto. El apoyo de la terapia ocupacional es fundamental para realizar adaptaciones y mantener la productividad.
El trastorno conductual del sueño REM (TCSR) es una afección en la que el paciente «representa» los sueños durante el sueño — puede dar patadas, golpes, gritar o caerse de la cama. Es altamente predictivo de neurodegeneración futura: aproximadamente el 75-90 % de los pacientes con TCSR idiopático presentan conversión a EP, atrofia multisistémica o demencia con cuerpos de Lewy a lo largo de 12-15 años en estudios de cohorte (Postuma 2019). Se considera un marcador de la fase prodrómica de la EP. Su reconocimiento es importante porque puede identificar la EP años antes de los síntomas motores y abrir ventanas para la intervención precoz.
La mayoría de los casos de EP (90-95 %) son esporádicos, sin antecedentes familiares claros. Las mutaciones genéticas identificadas (LRRK2, Parkin, PINK1, SNCA, GBA) explican solo el 10-15 % de los casos. El riesgo en familiares de primer grado de pacientes con EP esporádica es de 2-4 veces el de la población general — un aumento real, pero todavía bajo en términos absolutos. Las mutaciones del gen GBA (asociadas a la enfermedad de Gaucher) son el factor de riesgo genético más frecuente en la EP y pueden investigarse en pacientes con antecedentes familiares o inicio precoz.