¿Qué es la esclerosis múltiple?
La esclerosis múltiple (EM) es una enfermedad autoinmune crónica del sistema nervioso central (cerebro, médula espinal y nervios ópticos) en la que el sistema inmunitario ataca a la mielina — la capa protectora que envuelve las fibras nerviosas. Esta desmielinización altera la conducción de los impulsos nerviosos y produce una amplia variedad de síntomas neurológicos.
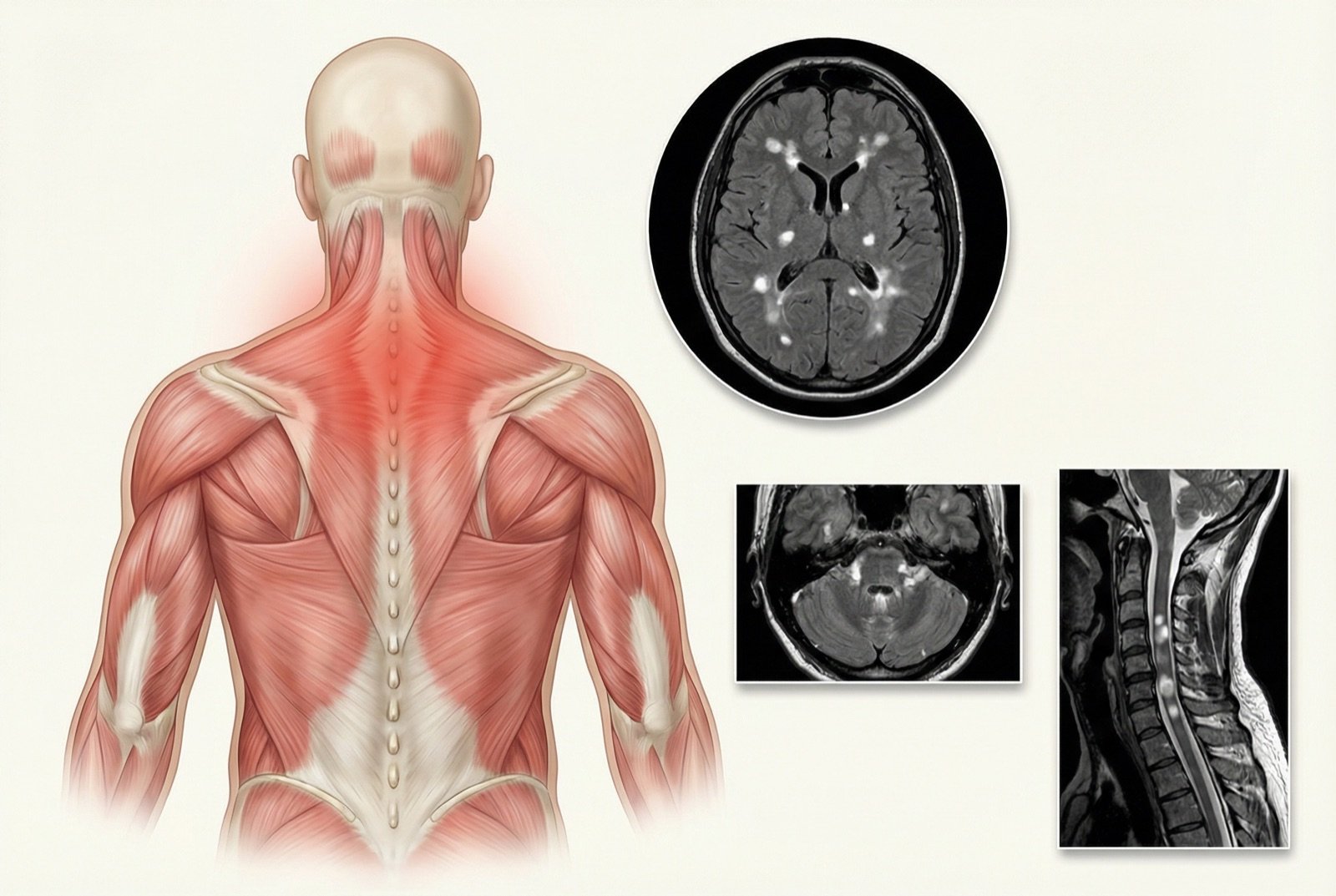
El nombre «esclerosis múltiple» se refiere a las múltiples áreas de cicatrización (esclerosis) que se forman en el cerebro y la médula espinal tras los episodios de inflamación y desmielinización. Estas lesiones, denominadas placas, pueden visualizarse mediante resonancia magnética y son la marca registrada de la enfermedad.
La EM afecta predominantemente a adultos jóvenes entre los 20 y los 40 años, con predominio femenino (2-3:1). Es la causa más frecuente de discapacidad neurológica no traumática en adultos jóvenes. La prevalencia varía notablemente según la región geográfica y es más alta en latitudes alejadas del ecuador.
Enfermedad autoinmune
El sistema inmunitario ataca por error a la mielina del sistema nervioso central, lo que causa inflamación, desmielinización y daño axonal progresivo.
Lesiones diseminadas
Placas de desmielinización en múltiples localizaciones del cerebro y la médula espinal, que producen síntomas neurológicos diversos e impredecibles.
Curso variable
La EM puede seguir distintos patrones — brotes y remisiones, progresión gradual o formas combinadas. El tratamiento precoz modifica significativamente la evolución.
Fisiopatología
La EM es una enfermedad inmunomediada en la que linfocitos T y B autorreactivos atraviesan la barrera hematoencefálica e inician una cascada inflamatoria contra los componentes de la mielina. La causa exacta que desencadena esta autoinmunidad sigue siendo desconocida, pero implica la interacción entre predisposición genética y factores ambientales.

Desmielinización y daño axonal
En la fase inflamatoria aguda (brote), los linfocitos T CD4+ y CD8+ infiltran el parénquima cerebral y liberan citocinas proinflamatorias, que activan macrófagos y microglía que fagocitan la mielina. Los anticuerpos producidos por los linfocitos B también contribuyen al daño. La desmielinización resultante bloquea o ralentiza la conducción de los impulsos nerviosos.
Además de la desmielinización, se produce daño axonal progresivo desde las fases iniciales de la enfermedad. La pérdida de mielina expone a los axones a estrés metabólico (incapacidad de mantener gradientes iónicos eficientemente), lo que conduce a la degeneración axonal. Es este daño axonal, y no la desmielinización en sí, el principal determinante de la discapacidad irreversible.
Factores de riesgo
Los factores de riesgo identificados incluyen: déficit de vitamina D (asociación fuerte con la latitud y la exposición solar), infección previa por el virus de Epstein-Barr (riesgo unas 32 veces mayor en individuos que seroconvierten al VEB durante el seguimiento), tabaquismo (aumenta el riesgo y acelera la progresión), obesidad en la adolescencia y factores genéticos (HLA-DRB1*15:01 y otros polimorfismos).
Síntomas
Los síntomas de la EM son extremadamente variables y dependen de la localización de las lesiones en el sistema nervioso central. Esta imprevisibilidad es una de las características más desafiantes de la enfermedad para pacientes y médicos.
🔍Síntomas habituales de la esclerosis múltiple
Inflamación del nervio óptico que provoca dolor al mover el ojo y pérdida visual. Con frecuencia es el primer síntoma de la EM, sobre todo en personas jóvenes.
Cansancio desproporcionado al esfuerzo, presente en hasta el 80 % de los pacientes. Es el síntoma más frecuente y uno de los más incapacitantes.
Hormigueo, adormecimiento o sensaciones anormales en los miembros o el tronco. Pueden afectar a áreas extensas o seguir un patrón en «banda» en el tronco.
Puede afectar a uno o más miembros. La debilidad de las piernas es la más frecuente y altera la marcha.
Aumento del tono muscular, especialmente en las piernas. Provoca rigidez, espasmos dolorosos y dificultad para la marcha.
Dificultad para coordinar los movimientos y mantener el equilibrio, por lesión cerebelosa o de las vías propioceptivas.
Urgencia, frecuencia e incontinencia urinarias en hasta el 80 % de los pacientes a lo largo de la enfermedad.
Dolor urente, lancinante o eléctrico (incluyendo neuralgia del trigémino), presente en el 50-70 % de los pacientes.
Dificultad de concentración, enlentecimiento del procesamiento de la información y alteración de la memoria en el 40-65 % de los pacientes. Con frecuencia se infravalora.
Sensación de descarga eléctrica que recorre la columna al flexionar el cuello — indica lesión en la médula cervical. Relativamente específico de la EM.
FORMAS CLÍNICAS DE LA ESCLEROSIS MÚLTIPLE
| FORMA | CARACTERÍSTICAS | FRECUENCIA |
|---|---|---|
| Remitente-recurrente (EMRR) | Brotes (episodios de nuevos síntomas o empeoramiento) seguidos de remisión parcial o completa. | 85 % al diagnóstico |
| Secundariamente progresiva (EMSP) | Progresión gradual de la discapacidad, con o sin brotes superpuestos. | Evoluciona a partir de la EMRR en el 50 % tras 15-20 años |
| Primariamente progresiva (EMPP) | Progresión gradual desde el inicio, sin brotes definidos. | 10-15 % de los casos |
| Progresiva-recurrente | Progresión desde el inicio con brotes superpuestos. | Rara (5 %) |
Diagnóstico
El diagnóstico de la EM se basa en los criterios de McDonald (revisados en 2017), que requieren la demostración de diseminación en el espacio (lesiones en múltiples localizaciones del SNC) y diseminación en el tiempo (lesiones en distintos momentos). La resonancia magnética es la prueba más importante para el diagnóstico.
🏥Pilares diagnósticos de la EM (criterios de McDonald 2017)
- 1.Diseminación en el espacio: lesiones en al menos 2 de 4 áreas típicas (periventricular, cortical/yuxtacortical, infratentorial, medular).
- 2.Diseminación en el tiempo: lesiones con y sin realce con gadolinio simultáneamente, o nueva lesión en T2/con realce en una RM posterior.
- 3.Resonancia magnética: múltiples lesiones en T2/FLAIR en localizaciones típicas. Patrón de referencia para demostrar la diseminación.
- 4.Líquido cefalorraquídeo: bandas oligoclonales presentes en el 95 % de los pacientes con EM (apoyan el diagnóstico, especialmente en formas progresivas).
- 5.Potenciales evocados: pueden demostrar desmielinización subclínica en las vías visuales, somatosensoriales o auditivas.
- 6.Exclusión de imitadores: neuromielitis óptica, lupus, sarcoidosis, vasculitis, déficit de vitamina B12.
Diagnóstico diferencial
La esclerosis múltiple es una de las enfermedades neurológicas con más imitadores clínicos. Un diagnóstico diferencial riguroso es esencial, ya que las terapias modificadoras de la enfermedad son específicas para la EM y no deben utilizarse en otras afecciones.
DIAGNÓSTICO DIFERENCIAL
Diagnóstico diferencial
Neuromielitis óptica (NMOSD)
- Neuritis óptica grave bilateral
- Mielitis transversa extensa
- Anti-AQP4 positivo
- La NMOSD tiene peor pronóstico — el diagnóstico diferencial es crucial.
Pruebas diagnósticas
- Anti-AQP4
- Anti-MOG
- RM de la columna
Lupus eritematoso sistémico
- Síntomas sistémicos
- ANA positivo
- Puede causar lesiones cerebrales
Pruebas diagnósticas
- ANA
- Anti-ADN de doble cadena
- Complemento
Sarcoidosis del SNC
- Lesiones del SNC con sarcoidosis sistémica
- ECA elevada
- Adenopatía hiliar
Pruebas diagnósticas
- ECA sérica
- PET-TC
- Biopsia
Leucoencefalopatía multifocal progresiva
- Inmunosuprimidos (VIH, uso de biológicos)
- Virus JC positivo
- Progresiva sin remisión
Pruebas diagnósticas
- PCR del virus JC en LCR
- RM
Migraña con aura
Leer más →- Episodios recurrentes con aura
- Sin déficit progresivo
- Cefalea asociada
Pruebas diagnósticas
- Criterios ICHD-3
- RM sin lesiones en T2
EM frente a neuromielitis óptica: una distinción crítica
La neuromielitis óptica (NMOSD) es el diagnóstico diferencial más importante de la EM, sobre todo porque su tratamiento es distinto y el uso inadvertido de ciertos inmunomoduladores de la EM (como natalizumab o fingolimod) puede empeorar la NMOSD. La NMOSD se caracteriza por neuritis óptica grave con pérdida visual intensa (con frecuencia bilateral), mielitis transversa extensa (lesiones que cubren 3 o más segmentos en la RM medular) y anticuerpo anti-AQP4 (acuaporina-4) positivo en el 70-80 % de los casos. El anti-MOG es positivo en una forma más benigna (MOGAD). La negatividad de ambos anticuerpos junto con una RM típica de EM orientan hacia el diagnóstico de EM.
El lupus eritematoso sistémico puede provocar manifestaciones neurológicas idénticas a las de la EM, incluidas lesiones cerebrales en la sustancia blanca, episodios de déficits neurológicos focales y alteraciones del LCR. La distinción se basa en la presencia de manifestaciones sistémicas (artritis, eritema malar, serositis, nefritis), ANA positivo a títulos altos, anti-ADN de doble cadena y descenso del complemento. En mujeres jóvenes con sospecha de EM, la investigación del lupus debe ser sistemática.
Leucoencefalopatía multifocal progresiva: alerta en pacientes inmunosuprimidos
La leucoencefalopatía multifocal progresiva (LMP), causada por el virus JC, es una complicación grave de los estados de inmunosupresión — incluidos los pacientes con EM en tratamiento con natalizumab u otros biológicos. Puede confundirse con un brote de EM o con la progresión de la enfermedad. Característicamente, la LMP es progresiva sin remisión, puede afectar al cerebelo y al tronco encefálico de forma asimétrica, y la RM muestra lesiones sin realce con contraste (a diferencia de los brotes activos de EM) con patrones específicos. La PCR del virus JC en el LCR es confirmatoria. En pacientes con EM en terapias de alta eficacia, cualquier nueva progresión debe levantar la sospecha de LMP.
La sarcoidosis del SNC es un imitador raro pero importante, especialmente cuando hay lesiones periventriculares en la RM similares a las placas de EM. La presencia de manifestaciones sistémicas (adenopatía hiliar bilateral, uveítis, lesiones cutáneas), enzima convertidora de angiotensina elevada y el patrón de las lesiones en la RM (tendencia a afectar meninges, pares craneales e hipotálamo) ayudan al diagnóstico. La biopsia de una lesión accesible (glándula salival, ganglio linfático) confirma con frecuencia la sarcoidosis sin necesidad de biopsia cerebral.
Migraña con aura: el imitador más frecuente
La migraña con aura es probablemente el diagnóstico que con más frecuencia se confunde con la EM, sobre todo en mujeres jóvenes. El aura migrañosa puede incluir síntomas visuales (escotoma centelleante), sensoriales (parestesias unilaterales) y del lenguaje, que se instauran de forma lenta y progresiva (característicamente en 5-20 minutos) y remiten espontáneamente en menos de 60 minutos. Las lesiones en sustancia blanca observadas en la RM de pacientes migrañosos (denominadas UBO — unidentified bright objects) pueden imitar las placas de EM, pero suelen ser más pequeñas, no presentan las localizaciones típicas de la EM y no aumentan con el tiempo.
La aplicación rigurosa de los criterios de McDonald 2017 — diseminación en el espacio (lesiones en las 4 regiones típicas) y en el tiempo — y el uso de bandas oligoclonales en el LCR son los elementos que distinguen la EM de la migraña con lesiones inespecíficas. La historia clínica detallada, incluyendo episodios previos de déficit neurológico, el patrón de los síntomas y los criterios diagnósticos de migraña (ICHD-3), es fundamental para el diagnóstico diferencial.
Tratamiento
El tratamiento de la EM comprende tres componentes: tratamiento de los brotes, terapias modificadoras de la enfermedad (DMT) para prevenir brotes y progresión, y tratamiento sintomático para el manejo de síntomas específicos como dolor, espasticidad y fatiga.
Tratamiento de los brotes
Los corticoides en dosis altas (metilprednisolona 1 g i.v. durante 3-5 días) son el tratamiento estándar de los brotes agudos. Aceleran la recuperación del brote por su efecto antiinflamatorio y la restauración de la barrera hematoencefálica, pero no modifican el grado final de recuperación. En los brotes resistentes a los corticoides puede indicarse plasmaféresis.
Terapias modificadoras de la enfermedad
Las DMT han revolucionado el tratamiento de la EM y reducen los brotes, las nuevas lesiones y la progresión de la discapacidad. Hay más de 20 DMT disponibles, con perfiles variables de eficacia y seguridad. La tendencia actual es iniciar con terapias de alta eficacia de forma precoz.
Las opciones incluyen terapias inyectables (interferones, acetato de glatirámero), orales (fingolimod, dimetilfumarato, teriflunomida, cladribina, siponimod) e infusiones (natalizumab, ocrelizumab, alemtuzumab, ofatumumab). La elección depende de la actividad de la enfermedad, el perfil de riesgo, las preferencias del paciente y la accesibilidad.
ABORDAJES TERAPÉUTICOS EN LA EM
| CATEGORÍA | EJEMPLOS | INDICACIÓN |
|---|---|---|
| Eficacia moderada | Interferones, acetato de glatirámero, teriflunomida, dimetilfumarato. | Formas leves a moderadas; pacientes con baja actividad de enfermedad. |
| Alta eficacia | Natalizumab, fingolimod, ocrelizumab, cladribina. | Enfermedad activa; pacientes con brotes frecuentes o lesiones activas en la RM. |
| Inducción | Alemtuzumab, trasplante de médula ósea. | Enfermedad muy activa, refractaria a terapias de alta eficacia. |
| Progresiva | Ocrelizumab (EMPP), siponimod (EMSP). | Formas progresivas — opciones limitadas pero crecientes. |
Tratamiento sintomático
El manejo de los síntomas es fundamental para la calidad de vida. Espasticidad: baclofeno, tizanidina, toxina botulínica. Dolor neuropático: pregabalina, gabapentina, amitriptilina. Fatiga: ejercicio físico regular (mejor evidencia), amantadina, modafinilo. Disfunción vesical: anticolinérgicos, toxina botulínica intravesical. La fisioterapia y la rehabilitación son componentes esenciales del tratamiento global.
Acupuntura como tratamiento
La acupuntura no es un tratamiento para la enfermedad en sí — las terapias modificadoras de la enfermedad son insustituibles para controlar la actividad inflamatoria de la EM. No obstante, la acupuntura se ha investigado como terapia complementaria para el manejo de síntomas como dolor, espasticidad, fatiga y disfunción vesical.
Estudios observacionales y pequeños ensayos clínicos sugieren un beneficio potencial para el dolor neuropático, la espasticidad y la fatiga en pacientes con EM. Los mecanismos propuestos incluyen modulación de la respuesta inmunitaria (efecto inmunomodulador), liberación de endorfinas para el alivio del dolor, regulación del tono muscular mediante modulación de los reflejos espinales y mejora de la calidad del sueño.
Es fundamental que la acupuntura se utilice como complemento del tratamiento convencional, nunca como sustituto. Los pacientes con EM que utilicen terapias complementarias deben mantener siempre las terapias modificadoras de la enfermedad prescritas por el neurólogo.
Pronóstico
El pronóstico de la EM es muy variable. Los factores pronósticos favorables incluyen sexo femenino, inicio con neuritis óptica o síntomas sensitivos, recuperación completa de los primeros brotes, baja carga lesional en la RM e inicio precoz de terapia de alta eficacia.
Las terapias modificadoras de la enfermedad han cambiado drásticamente el pronóstico de la EM. Los pacientes diagnosticados y tratados hoy tienen perspectivas significativamente mejores que los de hace dos décadas. La esperanza de vida, aunque ligeramente reducida (5-10 años), se está acercando a la de la población general con el tratamiento moderno.
La mayoría de los pacientes con EMRR mantiene la capacidad de marcha durante 20-25 años tras el diagnóstico. El concepto de «EM benigna» (discapacidad mínima a los 15 años) se aplica al 10-20 % de los pacientes, aunque ese grupo puede acabar progresando. La actividad física regular, no fumar y mantener niveles adecuados de vitamina D son factores modificables importantes.
Mitos y hechos
Mito frente a hecho
La esclerosis múltiple es una sentencia a la silla de ruedas.
Con los tratamientos modernos, la mayoría de los pacientes mantiene independencia funcional durante décadas. Las terapias modificadoras de la enfermedad han cambiado drásticamente el pronóstico.
Los pacientes con EM no deben hacer ejercicio.
El ejercicio físico regular se recomienda con firmeza y tiene beneficios demostrados sobre la fatiga, el ánimo, la fuerza muscular y la calidad de vida. Debe evitarse el calor excesivo.
EM y esclerosis lateral amiotrófica (ELA) son lo mismo.
Son enfermedades completamente distintas. La EM es autoinmune y afecta a la mielina. La ELA es neurodegenerativa y afecta a las motoneuronas. La EM tiene muchas opciones de tratamiento; la ELA, lamentablemente, todavía muy pocas.
La EM impide el embarazo.
Las mujeres con EM pueden tener gestaciones saludables. La tasa de brotes suele disminuir durante el embarazo (especialmente en el tercer trimestre). La planificación preconcepcional con el neurólogo es fundamental para ajustar la medicación.
Las dietas especiales curan la EM.
Ninguna dieta ha demostrado curar ni alterar significativamente la evolución de la EM. Una alimentación equilibrada y saludable es recomendable, pero no sustituye a las terapias modificadoras de la enfermedad.
Cuándo buscar ayuda
Preguntas frecuentes
Preguntas Frecuentes
No necesariamente. Con los tratamientos modernos, sobre todo las terapias modificadoras de la enfermedad de alta eficacia, la mayoría de los pacientes mantiene independencia funcional durante décadas. El pronóstico de la EM ha cambiado drásticamente en las últimas dos décadas. Los factores favorables incluyen inicio con neuritis óptica o síntomas sensitivos, sexo femenino, buena recuperación de los primeros brotes e inicio precoz del tratamiento. El acceso al tratamiento adecuado es el factor modificable más importante.
El consenso actual es iniciar el tratamiento lo antes posible. El concepto «treat early, treat effectively» se basa en la evidencia de que cada brote y cada nueva lesión en la RM representan daño que puede ser permanente. La ventana de oportunidad para preservar la función neurológica está en los primeros años de la enfermedad, cuando la capacidad de remielinización es mayor. Postergar el tratamiento no aporta beneficio y puede traducirse en acúmulo de discapacidad irreversible.
Sí. Las mujeres con EM pueden tener gestaciones saludables. La tasa de brotes suele disminuir durante el embarazo (especialmente en el tercer trimestre) y puede aumentar en los 3 meses tras el parto. La planificación preconcepcional con el neurólogo es fundamental para ajustar o suspender las terapias modificadoras (muchas están contraindicadas en la gestación). Algunas DMT más seguras durante el embarazo incluyen el acetato de glatirámero y los interferones. La lactancia materna también suele estar recomendada.
Sí. Existe una sólida evidencia epidemiológica que asocia el déficit de vitamina D con un mayor riesgo de desarrollar EM y con una actividad más agresiva de la enfermedad. La suplementación con vitamina D se recomienda para mantener niveles adecuados (por encima de 40-60 ng/mL). Aunque no es un tratamiento sustitutivo de las DMT, mantener niveles adecuados de vitamina D forma parte del cuidado integral del paciente con EM. La exposición solar moderada y la suplementación con vitamina D3 son estrategias sencillas y seguras.
Sí — se recomienda con firmeza. El ejercicio físico regular tiene beneficios demostrados sobre la fatiga, el ánimo, la fuerza muscular, la calidad de vida y la función cognitiva en pacientes con EM. La evidencia reciente sugiere que puede tener efectos neuroprotectores. El calor puede empeorar transitoriamente los síntomas (fenómeno de Uhthoff), pero no causa daño permanente. Se recomienda hacer ejercicio en ambientes frescos, mantener una hidratación adecuada y evitar el sobrecalentamiento. Actividades como la natación (en agua fría), el ciclismo y el pilates son excelentes opciones.
Sí. La fatiga de la EM es un síntoma específico e incapacitante presente en hasta el 80 % de los pacientes. Se caracteriza por agotamiento desproporcionado al esfuerzo realizado, empeora con el calor y al final del día, y no se alivia por completo con el reposo. Puede ser el síntoma más incapacitante incluso en pacientes con función motora preservada. Es distinta de la depresión (aunque pueden coexistir). El tratamiento incluye higiene del sueño, ejercicio físico regular (paradójicamente eficaz), amantadina y modafinilo.
Ninguna dieta ha demostrado curar ni alterar significativamente la evolución de la EM en ensayos clínicos sólidos. Una alimentación mediterránea equilibrada — rica en frutas, verduras, legumbres, cereales integrales, pescado y aceite de oliva, con limitación de carnes procesadas y azúcar — es recomendable por los mismos beneficios que aporta a la población general (salud cardiovascular, peso, microbiota intestinal). Las dietas muy restrictivas o los suplementos sin evidencia no deben sustituir al tratamiento con DMT.
Ante nuevos síntomas neurológicos o un empeoramiento significativo de los existentes que dure más de 24 horas, el paciente debe contactar a su neurólogo. Los brotes se tratan con metilprednisolona 1 g i.v. durante 3-5 días, lo que acelera la recuperación pero no modifica el grado final. El reposo adecuado y evitar el calor y las infecciones (que pueden precipitar pseudobrotes) son medidas de soporte. No suspenda la DMT durante el brote, salvo indicación expresa del neurólogo.
No hay evidencia de que la acupuntura interfiera con las DMT para la EM. Los efectos inmunomoduladores de la acupuntura parecen ser regulatorios (normalizadores), no estimulantes, y no se han descrito exacerbaciones de brotes asociadas al tratamiento. Los pacientes inmunosuprimidos deben informar al médico acupuntor para garantizar una asepsia adecuada durante las sesiones. La acupuntura puede utilizarse como complemento para el manejo de síntomas (fatiga, dolor, espasticidad), siempre con conocimiento del neurólogo.
La EM tiene componente genético, pero no se considera una enfermedad hereditaria en el sentido clásico. El riesgo para los hijos de una persona con EM es del 2-3 % (frente al 0,1-0,3 % de la población general) — es decir, 20-30 veces mayor, pero todavía bajo en términos absolutos. Para los hermanos, el riesgo es del 3-5 %. Los gemelos idénticos presentan una concordancia de solo el 25-30 %, lo que demuestra que los factores ambientales son tan importantes como los genéticos. No existe ninguna prueba genética que prediga el desarrollo de la EM.