¿Qué es la Neuropatía por Quimioterapia?
La neuropatía periférica inducida por quimioterapia (NPIQ) es una lesión de los nervios periféricos causada como efecto colateral de determinados agentes quimioterápicos. Es una de las complicaciones no hematológicas más frecuentes del tratamiento oncológico, y afecta hasta al 68 % de los pacientes en los primeros meses de quimioterapia.
Los agentes asociados con mayor frecuencia incluyen taxanos (paclitaxel, docetaxel), compuestos de platino (cisplatino, oxaliplatino, carboplatino), alcaloides de la vinca (vincristina), bortezomib y talidomida. Cada clase causa neuropatía por mecanismos distintos.
Además del impacto directo en la calidad de vida (dolor, pérdida de función, caídas), la NPIQ puede llevar a una reducción de dosis o a la interrupción prematura de la quimioterapia, comprometiendo potencialmente la eficacia del tratamiento oncológico. Es un desafío clínico significativo porque las opciones preventivas y terapéuticas son limitadas.
Alta Incidencia
Afecta hasta al 68 % de los pacientes en los primeros meses de quimioterapia. Puede persistir durante meses o años tras el término del tratamiento.
Mecanismos Variados
Cada clase de quimioterápico daña los nervios por mecanismos diferentes — daño mitocondrial, disrupción de microtúbulos o lesión del ganglio dorsal.
Impacto en el Tratamiento
Puede exigir reducción de dosis o interrupción de la quimioterapia, con potencial compromiso del resultado oncológico.
Fisiopatología
Los mecanismos de neurotoxicidad varían según la clase del quimioterápico, pero convergen en el daño a las neuronas sensoriales del ganglio de la raíz dorsal (DRG), a los axones periféricos o a ambos. El DRG resulta particularmente vulnerable por estar fuera de la barrera hematoencefálica.

MECANISMOS DE NEUROTOXICIDAD POR CLASE
| AGENTE | MECANISMO PRINCIPAL | PATRÓN CLÍNICO |
|---|---|---|
| Taxanos (paclitaxel) | Estabilización excesiva de microtúbulos, con bloqueo del transporte axonal | Neuropatía sensorial distal, dolor agudo (síndrome doloroso agudo del paclitaxel) |
| Platinos (cisplatino, oxaliplatino) | Daño al ADN y a las mitocondrias de las neuronas del ganglio dorsal | Neuronopatía sensorial, fenómeno de «coasting» tras la suspensión |
| Alcaloides de la vinca (vincristina) | Despolimerización de microtúbulos, disrupción del transporte axonal | Neuropatía sensoriomotora, estreñimiento (autonómica) |
| Bortezomib | Inhibición del proteasoma, acumulación de proteínas tóxicas en los nervios | Neuropatía sensorial dolorosa de fibras finas |
| Talidomida | Daño al ganglio dorsal e inhibición de la angiogénesis de los vasa nervorum | Neuropatía sensorial axonal, acumulativa |
Síntomas
La NPIQ se manifiesta predominantemente como una neuropatía sensorial distal simétrica, con un patrón en «calcetín y guante». Los síntomas sensoriales positivos (dolor, hormigueo) y negativos (entumecimiento, pérdida de sensibilidad) coexisten en grados variables.
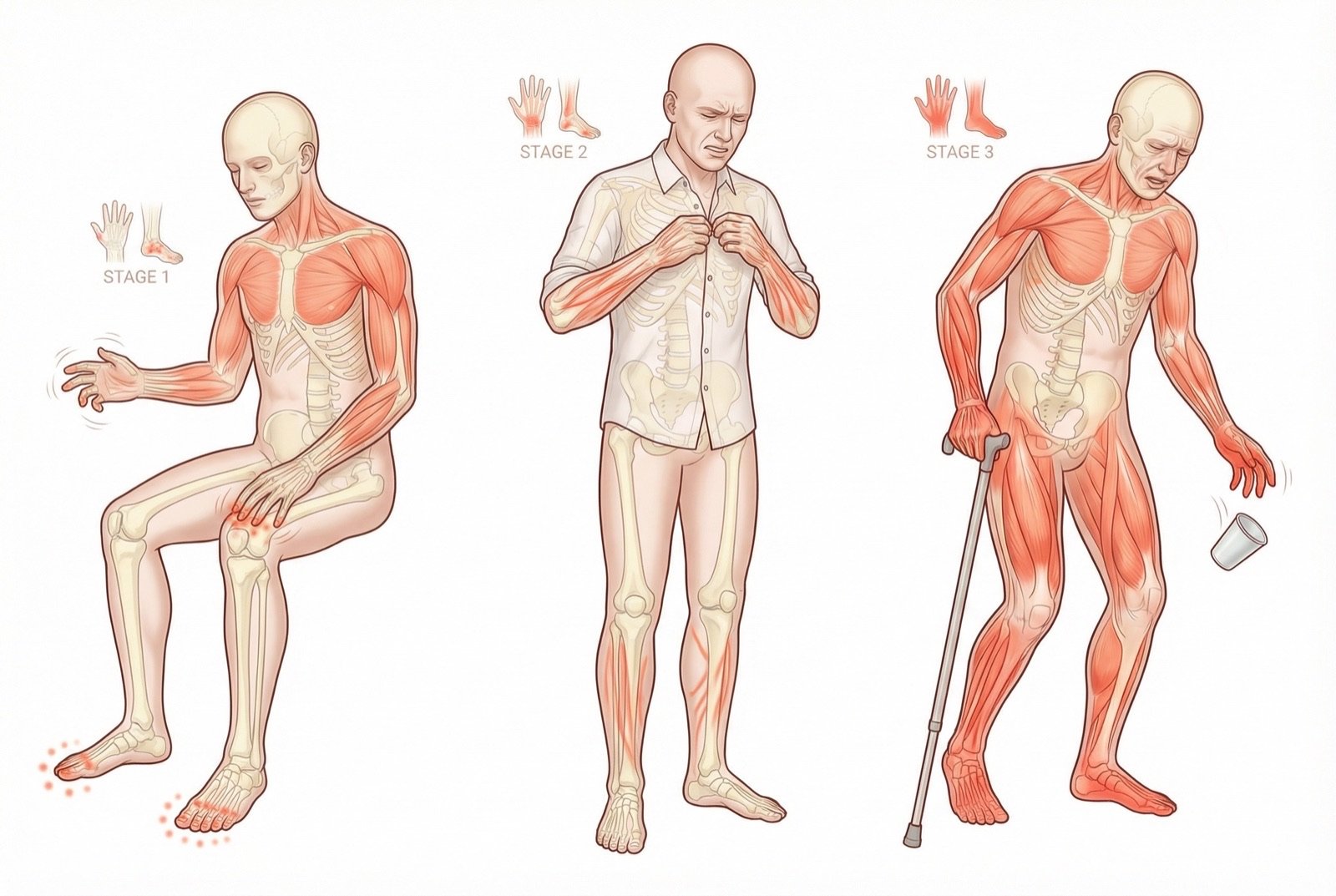
🔍Síntomas de la NPIQ
Típicamente simétricos, con inicio en las puntas de los dedos. Suele ser el primer síntoma percibido por el paciente.
Progresión en patrón de calcetín y guante. La pérdida de sensibilidad puede afectar la capacidad de abotonar, escribir o manipular objetos.
Dolor en ardor, descargas o punzadas, frecuentemente peor por la noche. Puede ser el síntoma más limitante.
Sensibilidad extrema al frío, incluido dolor al tocar objetos fríos o ingerir líquidos helados. Específica del oxaliplatino.
Dificultad para realizar tareas finas con las manos — abotonar, usar cierres, teclear. Impacto funcional significativo.
Pérdida de propiocepción en los pies, con aumento del riesgo de desequilibrio y caídas, especialmente en personas mayores.
Predomina con vincristina. Debilidad distal en los pies (pie caído) y manos (debilidad de prensión).
Diagnóstico
El diagnóstico de la NPIQ es clínico, basado en la relación temporal entre el inicio de la quimioterapia neurotóxica y la aparición de los síntomas neuropáticos. Es esencial establecer una evaluación neurológica basal antes del inicio de la quimioterapia para identificar neuropatía preexistente.
La gravedad se clasifica mediante la escala CTCAE (Common Terminology Criteria for Adverse Events) en grados de 1 a 4, que orientan las decisiones sobre ajuste de dosis. Una graduación precisa es fundamental para equilibrar el control oncológico y la calidad de vida.
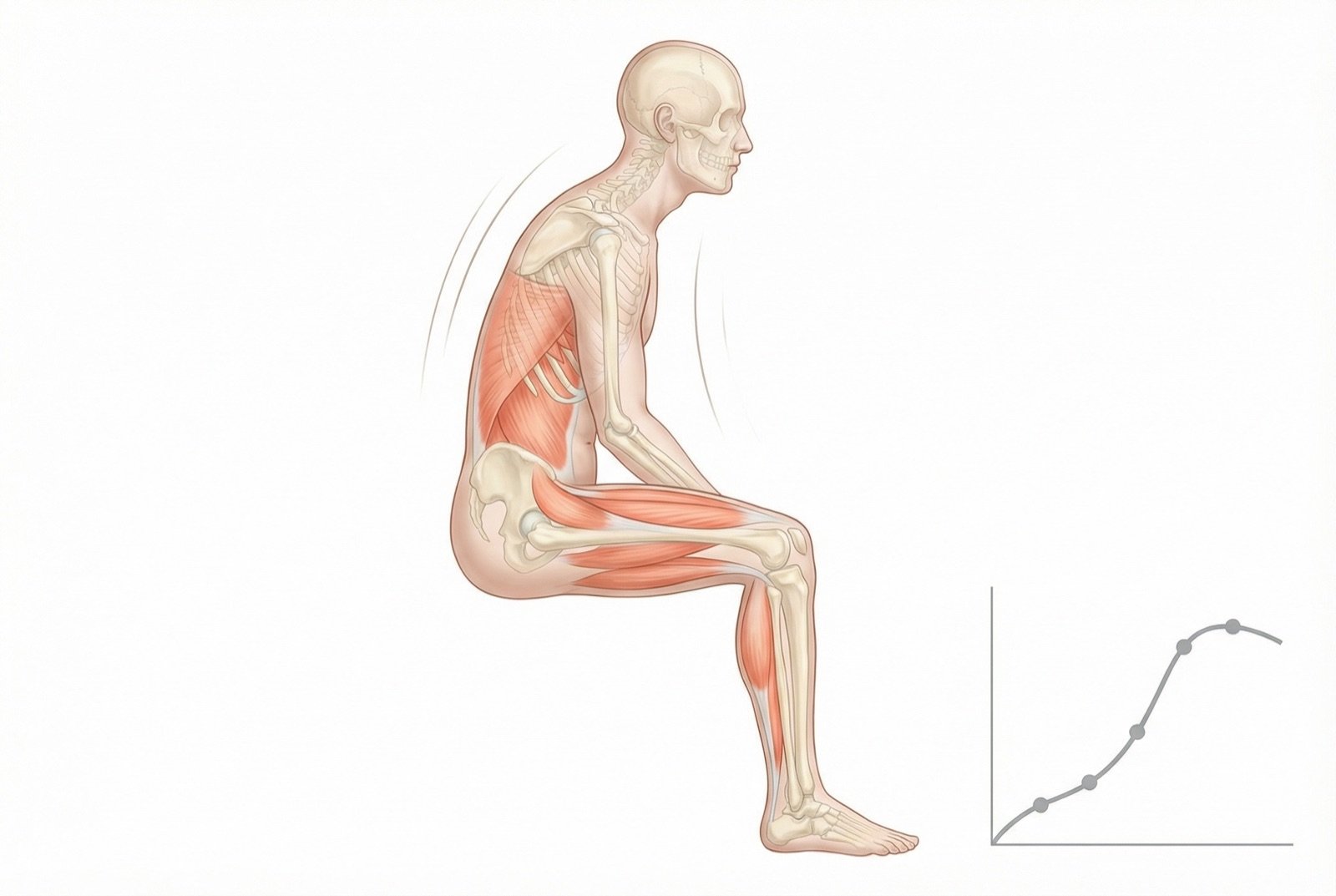
🏥Graduación de la NPIQ (CTCAE v5.0)
- 1.Grado 1: Asintomático, diagnosticado solo en el examen clínico. No requiere intervención.
- 2.Grado 2: Síntomas moderados, que limitan actividades instrumentales (cocinar, usar el ordenador). Considerar modificación de dosis.
- 3.Grado 3: Síntomas graves, que limitan actividades de autocuidado (vestirse, comer). Indicada suspensión o reducción significativa de dosis.
- 4.Grado 4: Consecuencias potencialmente mortales. Indicada suspensión inmediata del agente.
Diagnóstico Diferencial
No toda neuropatía en un paciente oncológico es causada por la quimioterapia. Las causas coexistentes o alternativas deben excluirse activamente, pues algunas son tratables y pueden agravar el cuadro.
DIAGNÓSTICO DIFERENCIAL
Diagnóstico diferencial
Neuropatía Diabética
Leer más →- DM2 preexistente
- Pies más afectados
- Progresión lenta
Pruebas diagnósticas
- Hemoglobina glucosilada
- EMG
Síndrome de Guillain-Barré
- Inicio agudo/subagudo
- Progresión rápida
- Arreflexia
- Progresión en días = ingreso urgente
Pruebas diagnósticas
- Punción lumbar
- EMG
Compresión de Raíz Nerviosa por Metástasis
- Dolor radicular en paciente oncológico
- Puede ser unilateral
- Progresión
- Déficit neurológico progresivo en oncológico = emergencia
Pruebas diagnósticas
- RM de columna
Deficiencia de B12 (por quimioterapia)
- Parestesias simétricas
- Anemia megaloblástica
- Lengua lisa
Pruebas diagnósticas
- Vitamina B12 sérica
- Hemograma
Neuropatía Paraneoplásica
- Asociada a anticuerpos anti-Hu, anti-Yo
- Puede preceder al diagnóstico oncológico
- Sensitiva predominante
Pruebas diagnósticas
- Anticuerpos paraneoplásicos
- PET-TC
NPIQ frente a Neuropatía Diabética Preexistente
Los pacientes diabéticos que inician quimioterapia constituyen un grupo de riesgo especial: la neuropatía diabética preexistente aumenta la vulnerabilidad de los nervios a los agentes neurotóxicos. Distinguir la contribución de cada causa resulta fundamental para el manejo. La relación temporal con el inicio de la quimioterapia, el empeoramiento abrupto y la distribución típica de las molestias (simétrica, distal, en «calcetín y guante») son elementos orientativos. La hemoglobina glucosilada y la electroneuromiografía (EMG) con estudio de conducción nerviosa ayudan a cuantificar el componente diabético.
Los pacientes que reciben agentes neurotóxicos con neuropatía de progresión más rápida de lo esperado, con componente motor prominente o con déficit asimétrico deben hacer sospechar una causa alternativa o coexistente — particularmente síndrome de Guillain-Barré, compresión por metástasis o neuropatía paraneoplásica.
Neuropatía Paraneoplásica: Diagnóstico Diferencial Crítico
La neuropatía paraneoplásica puede anteceder al diagnóstico oncológico en meses o años, y puede atribuirse erróneamente a la quimioterapia en pacientes ya en tratamiento. Se caracteriza por predominio sensitivo grave, afectación de los ganglios dorsales (neuronopatía sensitiva), progresión subaguda y, con frecuencia, presencia de anticuerpos onconeurales (anti-Hu, anti-Yo). El estudio con PET-TC puede revelar la neoplasia oculta.
La deficiencia de vitamina B12 se pasa por alto con frecuencia en pacientes oncológicos. Además del efecto de algunos quimioterápicos sobre la absorción de B12, la propia enfermedad oncológica y sus tratamientos pueden comprometer el estado nutricional. La determinación de B12 sérica debe incluirse en el estudio de toda neuropatía en paciente oncológico.
Cuándo Sospechar Compresión Medular por Metástasis
En el paciente oncológico con una neuropatía nueva, la compresión de raíz nerviosa por metástasis vertebral es una posibilidad que nunca debe descartarse sin evaluación adecuada. Los signos de alarma incluyen: dolor radicular de inicio reciente, asimetría marcada, progresión en días o semanas, síntomas urinarios o intestinales y dolor que empeora en decúbito. La RM de columna con contraste es la prueba de elección y debe solicitarse con urgencia ante estos signos.
La distinción entre NPIQ y compresión metastásica tiene implicaciones terapéuticas críticas: la compresión medular es una emergencia oncológica que requiere radioterapia urgente, corticosteroides en altas dosis y posible intervención quirúrgica. Cualquier demora en el diagnóstico puede resultar en déficit neurológico permanente.
Tratamiento
El manejo de la NPIQ es uno de los mayores desafíos en neurooncología. Las opciones terapéuticas comprobadas son limitadas, y la prevención (mediante monitorización y ajuste de dosis) sigue siendo la estrategia más importante.
Prevención
La Sociedad Americana de Oncología Clínica (ASCO) no recomienda ningún agente neuroprotector para la prevención rutinaria de la NPIQ. Vitaminas, antioxidantes, glutamina y calcio/magnesio no han demostrado eficacia consistente en ensayos aleatorizados. La prevención efectiva consiste en monitorización clínica rigurosa y ajuste de dosis cuando aparecen signos de neuropatía.
Tratamiento del Dolor Neuropático
La duloxetina (60 mg/día) es el único agente con evidencia clínica consistente para el tratamiento del dolor en la NPIQ establecida (Smith et al., JAMA 2013 — CALGB 170601; NNT ~6). La recomendación de la ASCO 2020 (Loprinzi et al., JCO) es moderada. La ASCO 2020 desaconseja explícitamente el uso rutinario de gabapentina (Rao 2007 — ensayo negativo); la amitriptilina también tuvo un ensayo negativo específico (Kautio 2008). La pregabalina puede intentarse caso por caso, con evidencia extrapolada de la neuropatía diabética.
Los abordajes no farmacológicos incluyen ejercicio físico (evidencia creciente de beneficio), fisioterapia, terapia ocupacional (para estrategias de compensación funcional) e intervenciones psicológicas (terapia cognitivo-conductual para el manejo del dolor).
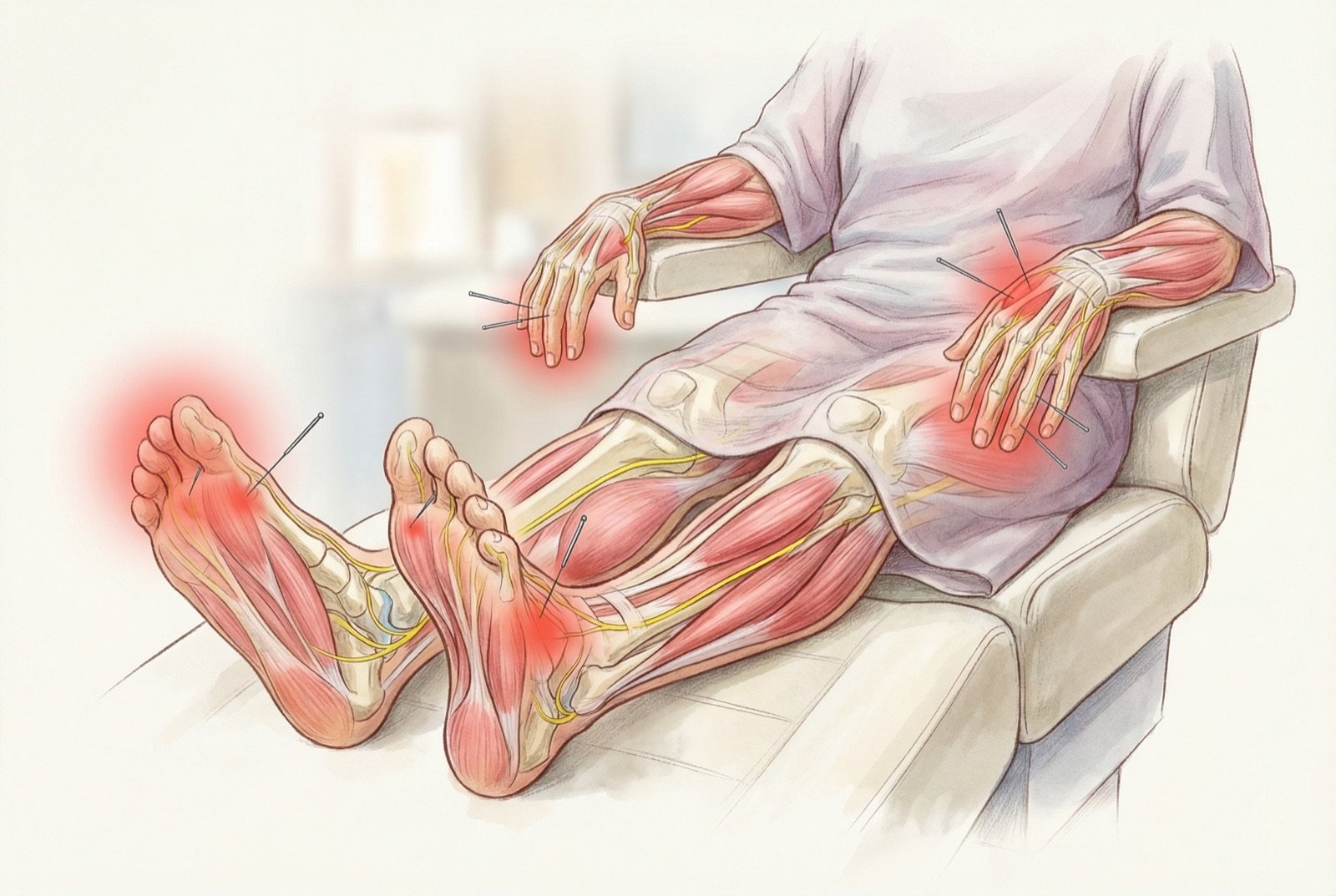
Acupuntura como Tratamiento
La acupuntura ha recibido atención creciente como terapia complementaria en la NPIQ, en parte porque las opciones farmacológicas son limitadas. Diversos centros oncológicos de referencia ya incorporan la acupuntura en sus servicios de medicina integrativa para pacientes con NPIQ.
Los estudios más relevantes para la NPIQ específicamente incluyen Bao et al. (Journal of the National Cancer Institute, 2020, n=75) y Molassiotis et al. (Cancer, 2019), ensayos aleatorizados que demostraron una mejoría significativa de los síntomas de neuropatía con acupuntura en comparación con controles (espera/sham). Los mecanismos propuestos incluyen mejoría de la microcirculación en los nervios periféricos, modulación de la transmisión nociceptiva en el asta dorsal y liberación de factores neurotróficos.
En pacientes oncológicos, la acupuntura suele ser bien tolerada cuando la realiza un médico acupunturista experimentado, con evaluación previa del recuento de plaquetas y neutrófilos. Como cualquier procedimiento, presenta riesgos (sangrado, infección) que deben sopesarse caso por caso. Puede ser particularmente útil en pacientes con respuesta parcial a la duloxetina o que no toleran la medicación. Los protocolos típicos contemplan sesiones semanales durante 8-12 semanas.
Pronóstico
El pronóstico de la NPIQ depende del agente causante, de la dosis acumulativa y de la gravedad en el momento de la suspensión. En general, la neuropatía inducida por taxanos tiende a mejorar gradualmente en los meses siguientes al término de la quimioterapia, aunque algunos pacientes mantienen síntomas residuales.
La neuropatía por compuestos de platino (especialmente cisplatino) tiene un pronóstico más reservado, con el fenómeno de «coasting» y una recuperación más lenta y a menudo incompleta. Los estudios de seguimiento a largo plazo muestran que el 30 % de los supervivientes de cáncer mantienen una neuropatía clínicamente significativa años después del tratamiento.
El impacto en la calidad de vida de los supervivientes de cáncer es sustancial — la NPIQ persistente afecta la movilidad, el sueño, la función manual y las actividades cotidianas. El reconocimiento de la NPIQ como una condición que requiere manejo crónico es fundamental para el cuidado integral de los supervivientes de cáncer.
Mitos y Hechos
Mito frente a hecho
La neuropatía siempre mejora cuando termina la quimioterapia
Aunque muchos pacientes mejoran, hasta el 30 % mantienen síntomas significativos meses o años después del tratamiento. Con cisplatino, la neuropatía puede incluso empeorar tras la suspensión (coasting).
Las vitaminas y suplementos previenen la NPIQ
Ningún suplemento ha demostrado eficacia en la prevención de la NPIQ en ensayos clínicos rigurosos. La ASCO no recomienda agentes neuroprotectores para la prevención rutinaria.
No hay nada que se pueda hacer para tratar el dolor
La duloxetina cuenta con evidencia robusta de eficacia para el dolor neuropático en la NPIQ. El ejercicio, la fisioterapia y la acupuntura son opciones complementarias con evidencia creciente.
Los síntomas en los pies durante la quimioterapia no necesitan reportarse
Comunicar los síntomas de manera precoz al oncólogo permite ajustes de dosis que pueden prevenir el daño nervioso permanente sin comprometer el resultado del tratamiento.
Cuándo Buscar Ayuda
Preguntas Frecuentes
Preguntas Frecuentes
No necesariamente. Con taxanos hay tendencia a una mejoría gradual en los meses siguientes. Con compuestos de platino (cisplatino, oxaliplatino), la neuropatía puede continuar empeorando durante semanas o meses tras la suspensión — fenómeno llamado «coasting». Los estudios de seguimiento muestran que cerca del 30 % de los supervivientes de cáncer mantienen neuropatía clínicamente significativa años después del tratamiento. La recuperación depende del agente utilizado, de la dosis acumulativa y de la gravedad en el momento de la suspensión.
Sí, siempre. Reportar los síntomas neuropáticos de manera precoz al oncólogo es la actitud más importante que el paciente puede tomar. La detección precoz permite ajustes de dosis o cambios de protocolo que pueden prevenir el daño nervioso permanente. No existe motivo para «aguantar» en silencio — el oncólogo necesita esa información para tomar decisiones terapéuticas informadas.
La evidencia actual no respalda el uso rutinario de ningún suplemento para la prevención de la NPIQ. La ASCO ha revisado extensamente los datos y no recomienda vitamina E, glutamina, calcio/magnesio, acetil-L-carnitina ni otros agentes para la prevención. Algunos suplementos, como la acetil-L-carnitina, han mostrado un resultado neutro o incluso negativo en estudios controlados. La prevención más eficaz es la monitorización clínica rigurosa con ajuste de dosis cuando es necesario.
Los ensayos aleatorizados en NPIQ específicamente (Bao et al., JNCI 2020; Molassiotis et al., Cancer 2019) demostraron mejoría de los síntomas de neuropatía con acupuntura en pacientes con NPIQ persistente, aunque los estudios son de tamaño modesto. Los mecanismos propuestos incluyen mejoría de la microcirculación en los nervios periféricos, modulación de la transmisión nociceptiva y liberación de factores neurotróficos. La acupuntura es reconocida por la Society for Integrative Oncology y por la ASCO como opción complementaria para el manejo de síntomas en oncología. Debe ser realizada por un médico acupunturista con experiencia en oncología integrativa.
Los más neurotóxicos son los compuestos de platino (cisplatino > oxaliplatino > carboplatino), los taxanos (paclitaxel > docetaxel), la vincristina, el bortezomib y la talidomida/lenalidomida. El cisplatino tiene la mayor neurotoxicidad acumulativa y el peor pronóstico de recuperación. El paclitaxel causa un síndrome doloroso agudo característico en los días posteriores a la infusión, además de neuropatía crónica.
Es una preocupación válida y uno de los principales dilemas clínicos en neurooncología. La reducción de dosis oportuna — realizada antes de la instalación de un daño grave — generalmente no compromete de manera significativa el resultado oncológico en la mayoría de los protocolos. La interrupción prematura por neuropatía grave, sin embargo, puede tener impacto. Por ello, la monitorización proactiva y el ajuste precoz de dosis (grados 2-3) son fundamentales para equilibrar eficacia oncológica y preservación neurológica.
El patrón más común es la neuropatía distal simétrica en «calcetín y guante», con predominio en pies y manos. No obstante, en casos graves puede progresar de manera proximal. La vincristina puede causar neuropatía autonómica (estreñimiento, retención urinaria). El cisplatino en altas dosis puede afectar la audición (ototoxicidad). Algunos pacientes desarrollan debilidad muscular distal, especialmente con vincristina.
El coasting es el fenómeno en que la neuropatía por compuestos de platino (especialmente cisplatino) continúa empeorando durante semanas o meses tras la suspensión del quimioterápico. Ocurre porque el daño primario es a los cuerpos celulares neuronales en el ganglio de la raíz dorsal, y la degeneración axonal progresa incluso después de la retirada del agente tóxico. Es diferente de la neuropatía por taxanos, que tiende a estabilizarse y mejorar tras la suspensión. El conocimiento de este fenómeno es crucial para la planificación terapéutica y para las expectativas de recuperación.
Sí, de manera significativa. La pérdida de propiocepción en los pies (sensación de posición) perjudica el equilibrio y la estabilidad postural. Los estudios muestran un riesgo de caídas 3-5 veces mayor en pacientes con NPIQ significativa. Las medidas preventivas incluyen fisioterapia con entrenamiento del equilibrio, uso de calzado adecuado con suela antideslizante, retirada de alfombras y objetos del suelo en casa, instalación de barras de apoyo en el baño e iluminación adecuada por la noche.
Depende del grado de la neuropatía y de la naturaleza del trabajo. La neuropatía leve (grado 1-2) generalmente permite mantener las actividades con adaptaciones. La pérdida de destreza manual puede afectar profesiones que exigen habilidades finas. La inestabilidad postural puede ser un problema en trabajos que requieren equilibrio u operación de equipos. La terapia ocupacional puede ayudar con estrategias de compensación y adaptación del entorno laboral para mantener la funcionalidad.
Leia Também
Aprofunde seu conhecimento com artigos relacionados