¿Qué es la neuropatía diabética?
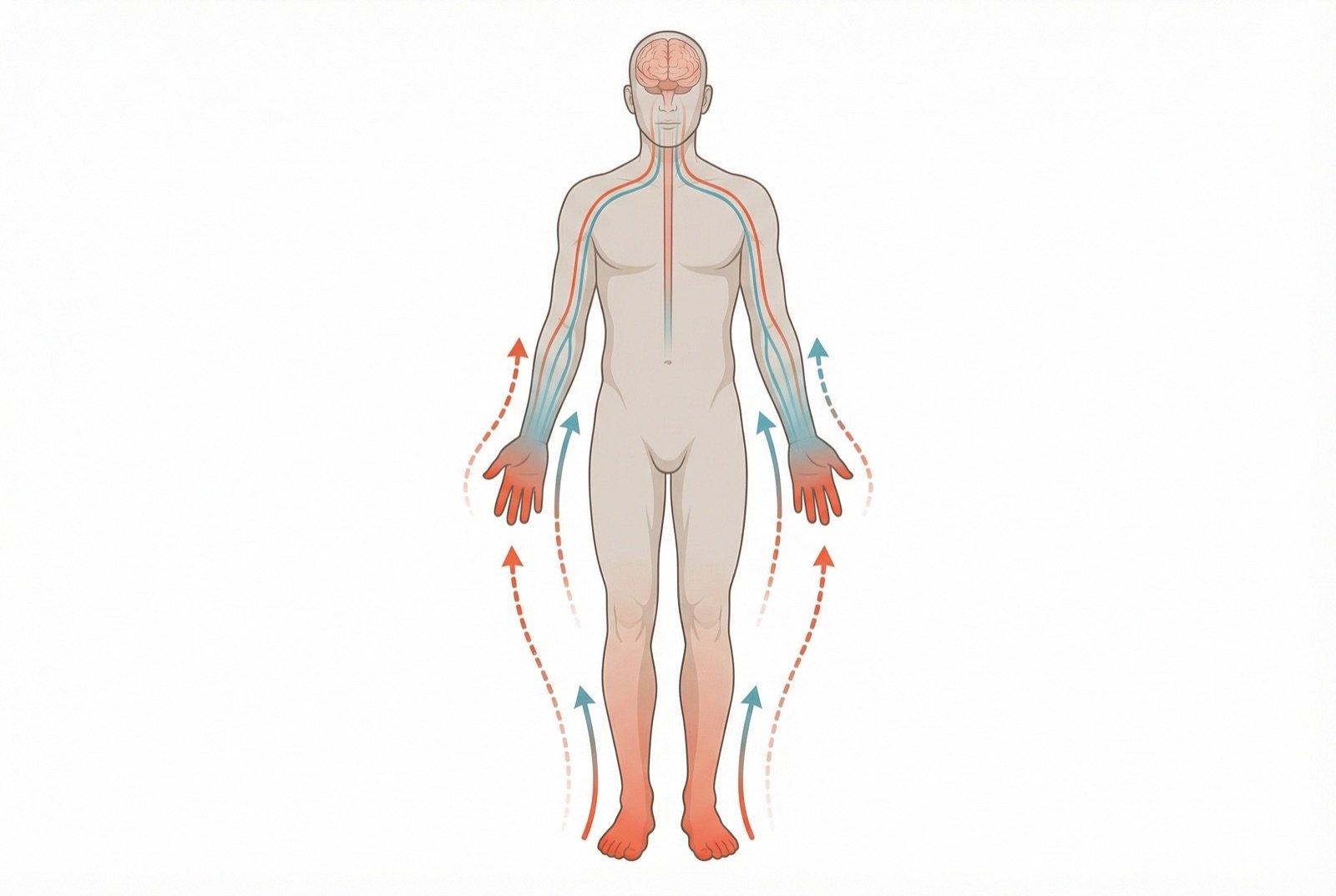
La neuropatía diabética es una lesión de los nervios periféricos provocada por la exposición crónica a niveles elevados de glucosa en la sangre. Es la complicación crónica más frecuente de la diabetes mellitus y afecta hasta al 50 % de los pacientes diabéticos a lo largo de la vida. Puede comprometer nervios sensitivos, motores y autónomos.
La forma más frecuente es la polineuropatía simétrica distal, que afecta predominantemente a los pies y a las piernas con un patrón «en calcetín y guante» y progresa de manera ascendente. Los síntomas varían desde hormigueo y adormecimiento leves hasta dolor neuropático intenso e incapacitante.
Más allá del dolor y la incomodidad, la neuropatía diabética es la principal causa de úlceras en los pies y de amputaciones no traumáticas. La pérdida de sensibilidad protectora en los pies permite que pequeñas lesiones pasen inadvertidas y evolucionen hacia úlceras e infecciones graves. El diagnóstico y el tratamiento precoces son esenciales para prevenir estas complicaciones devastadoras.
Alta prevalencia
Afecta hasta al 50 % de los pacientes diabéticos. Puede estar presente ya en el momento del diagnóstico de la diabetes tipo 2 e incluso en la prediabetes.
Pérdida de protección
La pérdida de sensibilidad en los pies es la principal causa de úlceras diabéticas y de amputaciones no traumáticas — una complicación prevenible.
Mecanismo metabólico
La hiperglucemia crónica daña directamente los nervios mediante estrés oxidativo, acumulación de sorbitol, glicación de proteínas y daño microvascular.
Fisiopatología
La neuropatía diabética resulta de una interacción compleja entre factores metabólicos y factores vasculares, ambos desencadenados por la hiperglucemia crónica. Estos mecanismos producen un daño progresivo de los axones y de las células de Schwann (productoras de mielina) y afectan en primer lugar a las fibras nerviosas más largas.

Mecanismos metabólicos
Vía del poliol: la hiperglucemia aumenta la actividad de la enzima aldosa reductasa, que convierte la glucosa en sorbitol. La acumulación de sorbitol provoca edema osmótico, depleción de mioinositol y reducción del glutatión (antioxidante), lo que genera estrés oxidativo y daño celular.
Productos finales de glicación avanzada (AGEs): la glucosa se une de forma no enzimática a proteínas estructurales de los nervios y altera su función. Los AGEs también activan receptores (RAGE) que desencadenan cascadas inflamatorias y de estrés oxidativo, dañando los axones y las células de Schwann.
Estrés oxidativo: la hiperglucemia incrementa la producción de radicales libres en las mitocondrias y supera la capacidad antioxidante de las células nerviosas. Se considera el mecanismo unificador central del daño neuropático diabético, que conecta todas las vías metabólicas.
Mecanismo vascular
Los nervios periféricos reciben aporte sanguíneo de pequeños vasos (vasa nervorum). La hiperglucemia provoca microangiopatía de los vasa nervorum — engrosamiento de la membrana basal, reducción de la luz vascular y disminución del flujo sanguíneo. La isquemia crónica resultante contribuye de forma significativa a la degeneración nerviosa.
Síntomas
La neuropatía diabética puede manifestarse de diversas formas, según el tipo de fibras nerviosas afectadas. La presentación más frecuente es la polineuropatía simétrica distal con síntomas sensitivos predominantes.
Síntomas de la neuropatía diabética
- 01
Hormigueo y adormecimiento en los pies
Parestesias distales que típicamente comienzan en los dedos de los pies y progresan de forma ascendente. Es el primer síntoma que percibe la mayoría de los pacientes.
- 02
Dolor en forma de ardor o sensación quemante
Dolor neuropático tipo ardor, frecuentemente peor por la noche y en reposo. Puede ser intenso e interferir con el sueño.
- 03
Descargas eléctricas espontáneas
Descargas dolorosas súbitas sin estímulo aparente, que reflejan actividad ectópica de los nervios dañados.
- 04
Alodinia
Dolor al tacto leve — el contacto de las sábanas con los pies por la noche puede resultar insoportable.
- 05
Pérdida de sensibilidad
Reducción progresiva de la sensibilidad táctil, térmica y dolorosa. El paciente puede no percibir lesiones en los pies.
- 06
Pérdida de equilibrio
Compromiso de la propiocepción (sensación de posición) en los pies, lo que aumenta el riesgo de caídas.
- 07
Debilidad muscular distal
En etapas avanzadas puede aparecer debilidad de los músculos intrínsecos del pie, con deformidades (dedos en garra).
- 08
Síntomas autonómicos
Hipotensión ortostática, gastroparesia, disfunción eréctil y anhidrosis en los pies (piel seca y agrietada).
FORMAS CLÍNICAS DE LA NEUROPATÍA DIABÉTICA
| FORMA | CARACTERÍSTICAS | PREVALENCIA |
|---|---|---|
| Polineuropatía simétrica distal | Patrón en calcetín y guante, simétrica, ascendente | La más frecuente (75 %) |
| Neuropatía autonómica | Cardiovascular, gastrointestinal, genitourinaria | Frecuente (hasta 50 %) |
| Neuropatía focal/multifocal | Mononeuropatía craneal, radiculopatía troncal | Menos frecuente |
| Amiotrofia diabética | Dolor y debilidad proximal en miembros inferiores | Rara (< 1 %) |
Diagnóstico
El diagnóstico de la neuropatía diabética combina la historia clínica, una exploración neurológica dirigida y, cuando es necesario, pruebas complementarias. Se recomienda el cribado anual en todos los pacientes con diabetes tipo 2 desde el momento del diagnóstico y en los pacientes con diabetes tipo 1 a partir de los 5 años de evolución de la enfermedad.
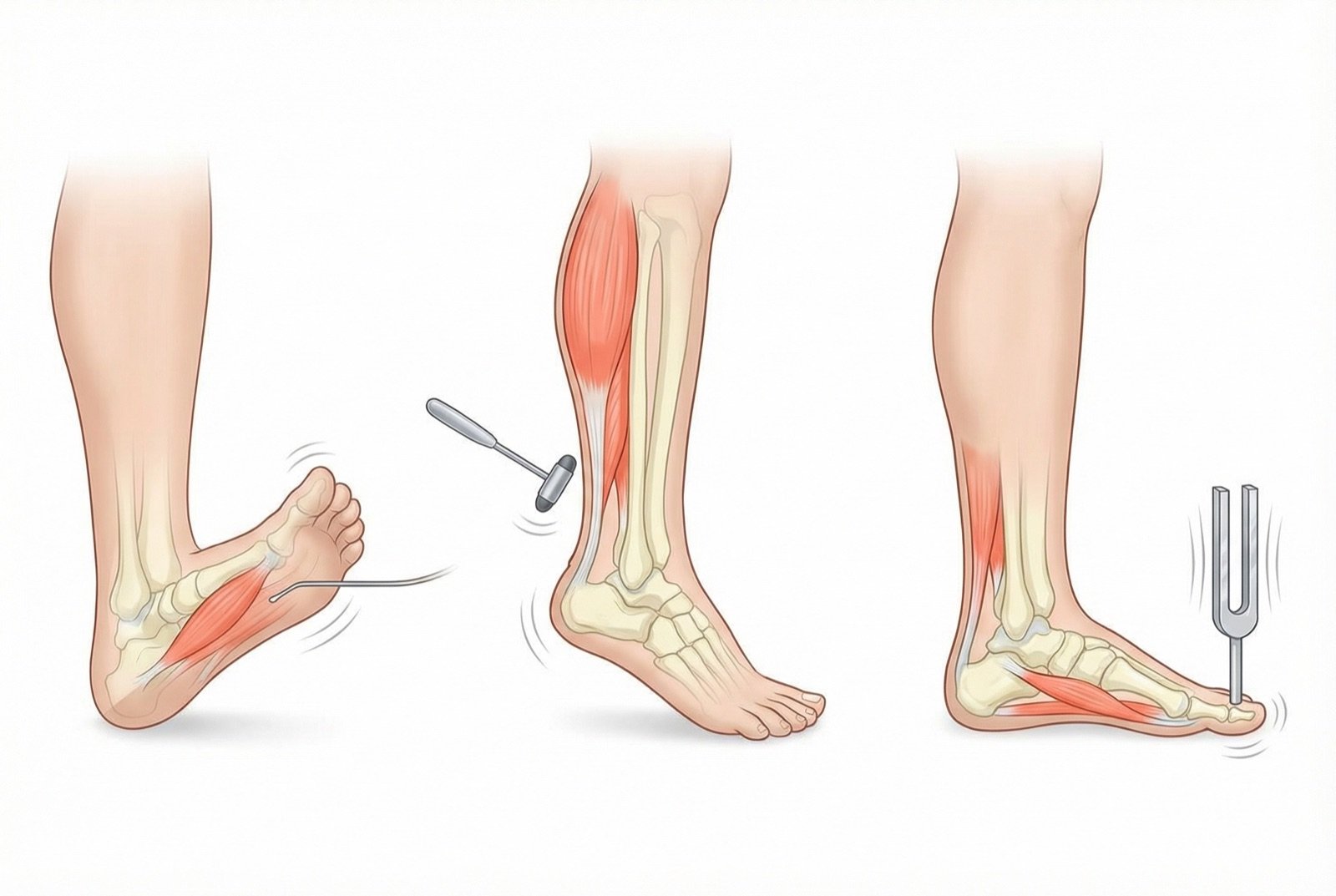
🏥Exploración neurológica de los pies — cribado
- 1.Prueba del monofilamento de 10 g (Semmes-Weinstein): evalúa la sensibilidad protectora. Su pérdida identifica riesgo de ulceración.
- 2.Prueba de sensibilidad vibratoria (diapasón de 128 Hz): se aplica en el hallux. Evalúa fibras gruesas mielinizadas.
- 3.Prueba de sensibilidad térmica: capacidad de diferenciar frío y calor en los pies.
- 4.Reflejos aquíleos: con frecuencia disminuidos o ausentes de manera precoz.
- 5.Prueba de sensibilidad con pinprick: evalúa fibras finas nociceptivas.
Diagnóstico diferencial
No toda neuropatía en un paciente diabético es causada por la diabetes. Las causas tratables de neuropatía deben excluirse activamente, porque pueden coexistir con la neuropatía diabética o ser la causa real de los síntomas.
DIAGNÓSTICO DIFERENCIAL
Diagnóstico diferencial
Síndrome del túnel carpiano
- Adormecimiento limitado al territorio del nervio mediano
- Phalen positivo
- Empeora por la noche
Pruebas diagnósticas
- EMG
Neuropatía alcohólica
- Patrón similar a la ND: distal, simétrica
- Consumo crónico de alcohol
- Deficiencia de vitamina B1
Pruebas diagnósticas
- Niveles de B1/B12
- GGT
- EMG
Hipotiroidismo
- Parestesias + fatiga + aumento de peso
- Reflejos lentos
- TSH elevada
Pruebas diagnósticas
- TSH
- T4 libre
Polirradiculoneuropatía desmielinizante inflamatoria crónica (PDIC)
- Debilidad predominante
- Progresión superior a 2 meses
- Líquido cefalorraquídeo con disociación albuminocitológica
- Debilidad progresiva = evaluación neurológica urgente
Pruebas diagnósticas
- Velocidad de conducción nerviosa
- Punción lumbar
Deficiencia de vitamina B12
- Neuropatía + anemia megaloblástica
- Glositis
- Vegetarianos/personas mayores
Pruebas diagnósticas
- B12 sérica
- Hemograma
Neuropatía diabética frente a otras neuropatías metabólicas
La neuropatía diabética es la causa más frecuente de neuropatía periférica en los países occidentales, pero coexiste con frecuencia con otras causas tratables. La deficiencia de vitamina B12 es particularmente relevante porque afecta hasta al 30 % de los pacientes diabéticos en tratamiento crónico con metformina — el fármaco reduce la absorción intestinal de B12 de forma dependiente de la dosis. El cuadro clínico puede ser similar al de la neuropatía diabética y la deficiencia de B12 mejora con frecuencia con la reposición adecuada, aunque el grado de recuperación depende de la duración y la gravedad del cuadro.
El hipotiroidismo es otra causa metabólica que se superpone con frecuencia — puede causar o agravar la neuropatía periférica y es más prevalente en pacientes diabéticos (especialmente mujeres). La determinación rutinaria de la TSH en todo paciente diabético con neuropatía es recomendable. El tratamiento con levotiroxina puede mejorar de forma significativa los síntomas neuropáticos cuando el hipotiroidismo es la causa o un factor contribuyente identificado.
Cuándo sospechar una neuropatía no diabética
Ciertos patrones deben aumentar la sospecha de que la neuropatía del paciente diabético tiene una causa adicional o alternativa. Una progresión rápida (de semanas a pocos meses), debilidad muscular prominente, neuropatía predominantemente motora, asimetría marcada, afectación de nervios craneales o una neuropatía que no se corresponde con el grado de control glucémico son signos de alarma.
La polirradiculoneuropatía desmielinizante inflamatoria crónica (PDIC) es más frecuente en diabéticos que en la población general y puede tener una presentación similar a la neuropatía diabética, pero con debilidad más prominente y velocidad de conducción nerviosa característicamente reducida. El diagnóstico correcto es fundamental porque la PDIC responde a inmunoglobulina intravenosa, plasmaféresis y corticoides — tratamientos que no tienen lugar en la neuropatía diabética.
Neuropatía alcohólica: la superposición frecuente
La neuropatía alcohólica tiene un patrón clínico prácticamente idéntico al de la neuropatía diabética — distal, simétrica y con afectación preferente de los pies. La coexistencia de diabetes y alcoholismo (no infrecuente) hace aún más difícil la distinción clínica. Elementos que apuntan hacia un componente alcohólico incluyen: deficiencia de tiamina (vitamina B1) documentada, antecedentes de consumo significativo de alcohol, GGT elevada y mejoría parcial con la abstinencia y la reposición vitamínica.
La evaluación analítica mínima en todo paciente con neuropatía periférica debe incluir: glucemia/HbA1c, TSH, B12, folato, función renal, hemograma y electroforesis de proteínas. Esta evaluación identifica las causas tratables más comunes y debe preceder a la atribución automática de toda neuropatía a la diabetes en pacientes diabéticos.
Tratamiento
El tratamiento de la neuropatía diabética se sostiene sobre tres pilares fundamentales: el control glucémico optimizado (la intervención con mayor impacto en la prevención de la progresión), el tratamiento del dolor neuropático y los cuidados de los pies.
Control glucémico
El control glucémico intensivo es la intervención con la evidencia más consistente para prevenir y retrasar la progresión de la neuropatía diabética. En la diabetes tipo 1, el estudio DCCT demostró una reducción del 60 % en el riesgo de neuropatía con control intensivo. En la diabetes tipo 2, el beneficio también existe, aunque resulta menos pronunciado.
La meta de hemoglobina glicada (HbA1c) debe individualizarse, pero en general se sitúa por debajo del 7 %. Las reducciones muy rápidas de la glucemia en pacientes con mal control crónico pueden, paradójicamente, causar neuropatía por tratamiento de la diabetes (dolor neuropático agudo transitorio).
Tratamiento del dolor neuropático
El dolor neuropático diabético no responde a los analgésicos comunes. Los fármacos de primera línea son: pregabalina (150-600 mg/día) y duloxetina (60-120 mg/día), ambos con sólida evidencia de eficacia. La gabapentina (900-3600 mg/día) y la amitriptilina (25-75 mg/día) son opciones de segunda línea.
La capsaicina tópica al 8 % (parche) está indicada para el dolor localizado. En casos refractarios pueden ser necesarios el tramadol u opioides fuertes, aunque con cautela. Las combinaciones de fármacos de clases diferentes (por ejemplo, pregabalina + duloxetina) pueden ser más eficaces que la monoterapia.
Base: control glucémico
HbA1c < 7 % (individualizada). Es la intervención con la evidencia más consistente para prevenir y retrasar la progresión. Control de los factores de riesgo cardiovascular asociados.
1.ª línea para el dolor: pregabalina o duloxetina
Iniciar con dosis baja y titular de forma gradual. Evaluar la eficacia en 4-8 semanas. Pregabalina: 75 mg 2 veces al día, hasta 300 mg 2 veces al día.
2.ª línea: gabapentina o amitriptilina
Indicadas cuando la primera línea es ineficaz o no se tolera. Amitriptilina: cautela en personas mayores y pacientes cardíacos.
Coadyuvantes: capsaicina tópica y combinaciones
Capsaicina al 8 % para dolor localizado. Combinaciones de fármacos de clases diferentes. Abordajes no farmacológicos.
Acupuntura como tratamiento
La acupuntura ha sido estudiada como terapia complementaria en la neuropatía diabética periférica, con resultados variables y aún limitados en algunos ensayos clínicos. Entre los mecanismos propuestos — basados predominantemente en estudios experimentales — figuran posibles efectos sobre la microcirculación, modulación central del dolor por vía opioide endógena e influencia sobre marcadores de estrés oxidativo; la traducción clínica de esos hallazgos todavía requiere evidencia más sólida.
Estudios experimentales en modelos animales de neuropatía diabética demuestran que la acupuntura puede mejorar la velocidad de conducción nerviosa y reducir marcadores de estrés oxidativo en los nervios periféricos. Los ensayos clínicos en humanos sugieren mejoría de los síntomas sensitivos y de la calidad de vida, aunque se necesitan estudios de mayor calidad.
La acupuntura puede considerarse como parte de un abordaje multimodal, especialmente en pacientes con respuesta parcial al tratamiento farmacológico o que presentan efectos adversos significativos. El control glucémico debe permanecer siempre como la base del tratamiento.
Pronóstico
La neuropatía diabética es una afección crónica y, en general, progresiva. Con un control glucémico adecuado la progresión puede retrasarse significativamente o estabilizarse. Sin embargo, la reversión del daño nervioso ya establecido es limitada, especialmente en formas avanzadas.
El impacto más relevante a largo plazo es el riesgo de ulceración y amputación de los pies. Los pacientes diabéticos con neuropatía tienen un riesgo anual de ulceración del 7 % y un riesgo de amputación entre 15 y 40 veces mayor que los diabéticos sin neuropatía. Los programas estructurados de cuidado de los pies reducen drásticamente estas complicaciones.
El dolor neuropático puede mejorar con el tiempo en algunos pacientes (a medida que las fibras nerviosas degeneran por completo), pero esto representa un empeoramiento de la neuropatía, no una mejoría. La pérdida progresiva de sensibilidad es el escenario más peligroso a largo plazo.
Mitos y hechos
Mito frente a hecho
El hormigueo en los pies es normal con la edad
El hormigueo persistente en los pies no es normal a ninguna edad. En pacientes diabéticos es un signo de alerta que debe investigarse como posible neuropatía.
Si no duele, no hay neuropatía
Hasta el 50 % de los pacientes con neuropatía diabética son asintomáticos. La forma indolora con pérdida de sensibilidad es, en realidad, la más peligrosa, porque aumenta el riesgo de úlceras.
La neuropatía solo aparece en la diabetes avanzada
Puede estar presente ya en el momento del diagnóstico de la diabetes tipo 2 (porque la hiperglucemia puede preceder al diagnóstico durante años) e incluso en la prediabetes.
Los analgésicos comunes resuelven el dolor neuropático
El dolor neuropático no responde adecuadamente a los analgésicos simples ni a los antiinflamatorios. Requiere fármacos específicos como pregabalina, duloxetina o gabapentina.
No hay nada que hacer — la neuropatía solo empeora
Un control glucémico adecuado puede prevenir y retrasar significativamente la progresión. Los tratamientos para el dolor son eficaces. Los cuidados de los pies previenen complicaciones graves.
Cuándo buscar ayuda
Preguntas frecuentes
Preguntas Frecuentes
En fases iniciales, el control glucémico intensivo puede llevar a una mejoría parcial de la neuropatía, especialmente de los síntomas. Sin embargo, los daños establecidos en los axones difícilmente se revierten — el objetivo principal del control glucémico es prevenir la progresión, no revertir daños ya instaurados. En la diabetes tipo 1, el estudio DCCT demostró una reducción del 60 % en el riesgo de neuropatía con control intensivo. La ventana de oportunidad para una prevención eficaz se sitúa en los primeros años de diabetes.
El dolor neuropático diabético clásicamente empeora en reposo y por la noche por varios mecanismos: ausencia de los estímulos sensoriales diurnos que «distraen» al sistema nervioso central, descenso de la temperatura de los pies al dormir (que puede exacerbar la actividad ectópica de los nervios dañados) y, posiblemente, el ritmo circadiano de los mediadores inflamatorios. El empeoramiento nocturno es una característica que distingue al dolor neuropático del dolor muscular o articular, que en general empeora con el uso.
Sí, la gran mayoría de las úlceras y amputaciones del pie diabético son prevenibles. Las medidas esenciales incluyen: inspección diaria de los pies (especialmente entre los dedos), hidratación con crema en los talones, uso de calzado adecuado sin costuras internas (preferir zapatos con puntera ancha), calcetines sin elástico constrictivo, consulta podológica regular y cribado anual con monofilamento para detectar la pérdida de sensibilidad protectora. La educación del paciente sobre el cuidado de los pies es la intervención con mayor impacto en la prevención de amputaciones.
La metformina por sí sola no causa neuropatía, pero reduce la absorción de vitamina B12 en el intestino delgado de forma dependiente de la dosis y del tiempo. La deficiencia de B12 puede aparecer en hasta el 30 % de los usuarios crónicos de metformina y puede causar o agravar la neuropatía periférica. Por ello, se recomienda la determinación periódica de vitamina B12 en pacientes en tratamiento prolongado con metformina, especialmente con dosis superiores a 1500 mg/día. La reposición de B12 es sencilla y eficaz.
La acupuntura ha sido estudiada como complemento en el tratamiento del dolor neuropático diabético, con resultados variables en ensayos clínicos y evidencia aún limitada. Entre los mecanismos propuestos — derivados mayoritariamente de estudios experimentales — figuran posibles efectos sobre la microcirculación, modulación central del dolor por vía opioide endógena e influencia sobre marcadores de estrés oxidativo. El médico acupunturista puede considerar la acupuntura como coadyuvante al tratamiento farmacológico, especialmente en pacientes con respuesta parcial a pregabalina o duloxetina. El control glucémico permanece como pilar fundamental del tratamiento.
Ambas son de primera línea con eficacia similar. La elección depende del perfil del paciente: la duloxetina se prefiere en pacientes con depresión concomitante (trata ambas afecciones), obesidad (puede provocar una leve pérdida de peso) o que ya utilizan otros medicamentos sedantes. La pregabalina resulta más útil cuando hay insomnio asociado (efecto hipnótico útil), ansiedad generalizada o cuando la duloxetina no se ha tolerado. La combinación de ambas puede ser más eficaz que la monoterapia en casos refractarios.
La pérdida de sensibilidad protectora en la neuropatía diabética tiende a ser progresiva sin un control glucémico adecuado. Con un control metabólico optimizado, la progresión puede retrasarse mucho o estabilizarse. La recuperación significativa de la sensibilidad de las fibras gruesas es menos común en adultos con neuropatía establecida, aunque en diabéticos tipo 1 con muy buen control existen datos de recuperación parcial. Las fibras finas (que median la temperatura y el dolor) pueden mostrar más plasticidad que las gruesas.
Sí, la neuropatía autonómica diabética puede tener consecuencias graves. La neuropatía cardiovascular autonómica aumenta el riesgo de muerte súbita y de infarto silencioso (sin dolor, porque las fibras nociceptivas cardíacas están dañadas). La hipotensión ortostática puede provocar caídas y síncopes. La gastroparesia perjudica el control glucémico. La disfunción eréctil afecta a la calidad de vida. La vejiga neurógena aumenta el riesgo de infecciones urinarias. El cribado sistemático de estas complicaciones forma parte del cuidado integral del paciente diabético.
No existe un umbral absoluto — el riesgo de neuropatía aumenta de forma continua con el tiempo de exposición a la hiperglucemia. El principal predictor es la hemoglobina glicada (HbA1c) media a lo largo de los años. Cada 1 % de reducción en la HbA1c crónicamente elevada se asocia a una reducción significativa del riesgo de complicaciones neuropáticas. Importante: la neuropatía puede estar presente ya en la prediabetes (HbA1c 5,7-6,4 %), cuando la glucemia aún no alcanza los criterios de diabetes, lo que subraya la importancia del cribado precoz.
Sí, la inspección diaria de los pies es una de las medidas preventivas más importantes y de menor coste. El paciente debe verificar: presencia de ampollas, cortes, fisuras, callosidades, enrojecimiento, calor localizado, deformidades o cambios de color. Los pacientes con dificultad visual o movilidad reducida deben usar un espejo o pedir ayuda a un familiar. Cualquier lesión, por pequeña que sea, debe comunicarse al médico de inmediato — en el pie diabético insensible, las pequeñas lesiones que pasan desapercibidas evolucionan rápidamente a úlceras profundas.
Lea También
Profundice su conocimiento con artículos relacionados